uitsluitend voor onderzoeksdoeleinden
Semaxanib (SU5416) VEGFR2-remmer
Cat.Nr.S2845
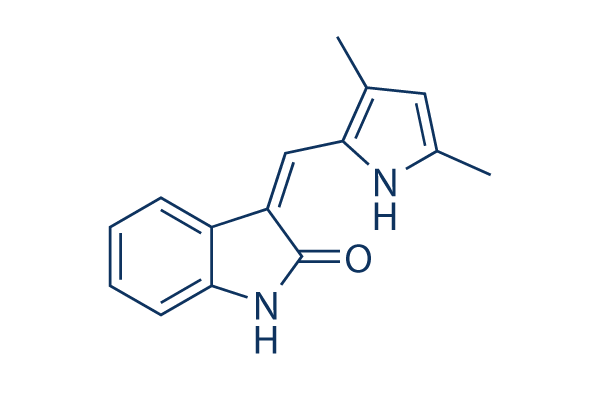
Chemische structuur
Moleculair gewicht: 238.28
Kwaliteitscontrole
| Gerelateerde doelwitten | EGFR PDGFR FGFR c-Met Src MEK CSF-1R FLT3 HER2 c-Kit |
|---|---|
| Overige VEGFR Inhibitoren | SAR131675 SU 5402 Cediranib (AZD2171) Vatalanib (PTK787) 2HCl Anlotinib (AL3818) Dihydrochloride Linifanib (ABT-869) Apatinib (YN968D1) Apatinib (YN968D1) mesylate Ki8751 ZM 323881 HCl |
Celkweek, behandeling & werkconcentratie
| Cellijnen | Assaytype | Concentratie | Incubatietijd | Formulering | Activiteitsbeschrijving | PMID |
|---|---|---|---|---|---|---|
| MCF7 cells | Cytotoxicity assay | 48 h | Cytotoxicity against human MCF7 cells after 48 hrs by CCK8 assay, IC50=3.1 nM | |||
| mouse B16F10 cells | Cytotoxicity assay | 48 h | Cytotoxicity against mouse B16F10 cells after 48 hrs by CCK8 assay, IC50=3.6 nM | |||
| human U251 cells | Function assay | Inhibition of VEGFR2 in human U251 cells by phosphotyrosine ELISA, IC50=12.9 nM | ||||
| human A431 cells | Function assay | Antiangiogenic activity against human A431 cells, IC50=0.085 μM | ||||
| CHO cells | Function assay | Inhibition of VEGFR induced autophosphorylation of human Vascular endothelial growth factor receptor 2 (VEGFR2) transfected in CHO cells, IC50=0.884 μM | ||||
| human MCF7 cells | Proliferation assay | 4 days | Antiproliferative activity against human MCF7 cells after 4 days by coulter counter method, IC50=1.9 μM | |||
| human SF539 cells | Function assay | Inhibition of PDGFRbeta in human SF539 cells by phosphotyrosine ELISA, IC50=2.4 μM | ||||
| A431 cells | Function assay | Inhibition of VEGFR2 expressed in human A431 cells, IC50=12.9 μM | ||||
| HUVEC cells | Proliferation assay | 72 h | Antiproliferative activity against human HUVEC cells assessed as reduction in cell viability after 72 hrs by trypan blue assay, GI50=13.6 μM | |||
| human HMEC1 cells | Proliferation assay | 7 days | Antiproliferative activity against human HMEC1 cells after 7 days by coulter counter method, IC50=15 μM | |||
| human HeLa cells | Proliferation assay | 4 days | Antiproliferative activity against human HeLa cells after 4 days by coulter counter method, IC50=20 μM | |||
| Klik om meer experimentele gegevens over de cellijn te bekijken | ||||||
Chemische informatie, Opslag en Stabiliteit
| Moleculair gewicht | 238.28 | Formule | C15H14N2O |
Opslag (Vanaf de ontvangstdatum) | |
|---|---|---|---|---|---|
| CAS-nr. | 204005-46-9 | SDF downloaden | Opslag van stamoplossingen |
|
|
| Synoniemen | semaxinib | Smiles | CC1=CC(=C(N1)C=C2C3=CC=CC=C3NC2=O)C | ||
Oplosbaarheid
|
In vitro |
DMSO
: 17 mg/mL
(71.34 mM)
Ethanol : 2 mg/mL Water : Insoluble |
Molariteitscalculator
|
In vivo |
|||||
In vivo Formuleringscalculator (Heldere oplossing)
Stap 1: Voer de onderstaande informatie in (Aanbevolen: Een extra dier voor het geval van verlies tijdens het experiment)
Stap 2: Voer de in vivo formulering in (Dit is alleen de calculator, geen formulering. Neem eerst contact met ons op als er geen in vivo formulering is in het gedeelte Oplosbaarheid.)
Berekeningsresultaten:
Werkconcentratie: mg/ml;
Methode voor het bereiden van DMSO-mastervloeistof: mg geneesmiddel vooraf opgelost in μL DMSO ( Concentratie mastervloeistof mg/mL, Neem eerst contact met ons op als de concentratie de DMSO-oplosbaarheid van de partij geneesmiddel overschrijdt. )
Methode voor het bereiden van in vivo formulering: Neem μL DMSO mastervloeistof, voeg vervolgens toeμL PEG300, mengen en helder maken, voeg vervolgens toeμL Tween 80, mengen en helder maken, voeg vervolgens toe μL ddH2O, mengen en helder maken.
Methode voor het bereiden van in vivo formulering: Neem μL DMSO mastervloeistof, voeg vervolgens toe μL Maïsolie, mengen en helder maken.
Opmerking: 1. Zorg ervoor dat de vloeistof helder is voordat u het volgende oplosmiddel toevoegt.
2. Zorg ervoor dat u het/de oplosmiddel(en) in de juiste volgorde toevoegt. U moet ervoor zorgen dat de verkregen oplossing, bij de vorige toevoeging, een heldere oplossing is voordat u verdergaat met het toevoegen van het volgende oplosmiddel. Fysische methoden zoals vortexen, echografie of een warmwaterbad kunnen worden gebruikt om het oplossen te bevorderen.
Werkingsmechanisme
| Targets/IC50/Ki |
VEGFR2/Flk1
(Cell-free assay) 1.23 μM
|
|---|---|
| In vitro |
Semaxanib (SU5416) remt VEGF-afhankelijke fosforylering van de Flk-1-receptor in Flk-1-overexpressende NIH 3T3-cellen met een IC50 van 1,04 μM, en PDGF-afhankelijke autofosforylering in NIH 3T3-cellen met een IC50 van 20,3 μM. Het remt ook VEGF- en FGF-gestuurde mitogenese op een dosisafhankelijke manier met respectievelijk een IC50 van 0,04 en 50 μM. Behandeling met deze verbinding heeft geen effect op de in vitro groei van C6-glioom-, Calu 6-longcarcinoom-, A375-melanoom-, A431-epidermoïde carcinoom- en SF767T-glioomcellen (alle IC50s > 20 μM).
|
| Kinase Assay |
Biochemische kinase assays
|
|
Gesolubiliseerde membranen van 3T3 Flk-1-cellen worden toegevoegd aan polystyreen ELISA-platen die waren voorbekleed met een monoklonaal antilichaam dat Flk-1 herkent. Na een nacht incuberen met lysaat bij 4 °C, worden seriële verdunningen van Semaxanib (SU5416) toegevoegd aan de geïmmunolocaliseerde receptor. Om autofosforylering van de receptor te induceren, worden verschillende concentraties ATP toegevoegd aan de ELISA-plaatputjes die serieel verdunde oplossingen van deze verbinding bevatten. De autofosforylering mag gedurende 60 minuten bij kamertemperatuur doorgaan en wordt vervolgens gestopt met EDTA. De hoeveelheid fosfotyrosine die aanwezig is op de Flk-1-receptoren in de individuele putjes wordt bepaald door de geïmmunolocaliseerde receptor te incuberen met een gebiotinyleerd monoklonaal antilichaam gericht tegen fosfotyrosine. Na verwijdering van het ongebonden anti-fosfotyrosine antilichaam, wordt avidine-geconjugeerd mierikswortelperoxidase H toegevoegd aan de putjes. Een gestabiliseerde vorm van 3,3',5,5'-tetramethylbenzidinedihydrochloride en H2O2 wordt aan de putjes toegevoegd. De kleuruitlezing van de assay mag gedurende 30 minuten ontwikkelen en de reactie wordt gestopt met H2SO4.
|
|
| In vivo |
Semaxanib (SU5416) remt de groei van A375-tumoren in vivo dosisafhankelijk. Een >85% remming van de subcutane tumorgroei wordt waargenomen bij dagelijkse i.p. toediening van deze verbinding in DMSO, zonder meetbare toxiciteit. Het vertoont een breed spectrum van antitumoractiviteit, waarbij de subcutane groei van 8 van de 10 geteste tumorlijnen (A431, Calu-6, C6, LNCAP, EPH4-VEGF, 3T3HER2, 488G2M2 en SF763T-cellen) significant wordt geremd met een gemiddelde mortaliteit van 2,5%. Bij 25 mg/kg/dag vertoont het een krachtige antiangiogene activiteit, wat resulteert in een significante vermindering van zowel de totale als de functionele vasculaire dichtheid van de tumormicrovasculatuur.
|
Referenties |
|
Toepassingen
| Methoden | Biomarkers | Afbeeldingen | PMID |
|---|---|---|---|
| Western blot | p-VEGFR2 / VEGFR2 / p-PLCγ1 / PLCγ1 / p-ERK / ERK |
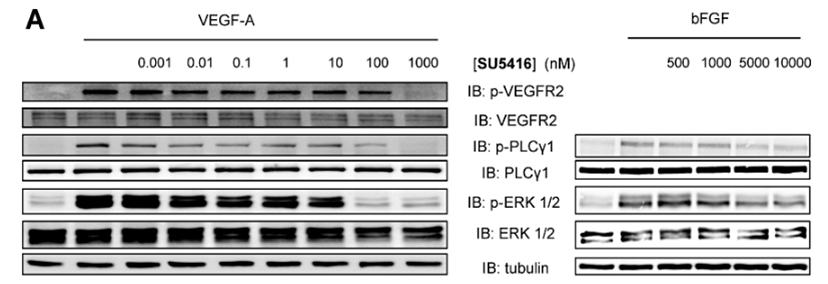
|
21699503 |
| Immunofluorescence | CD31 / OCT-4 / SOX-2 |
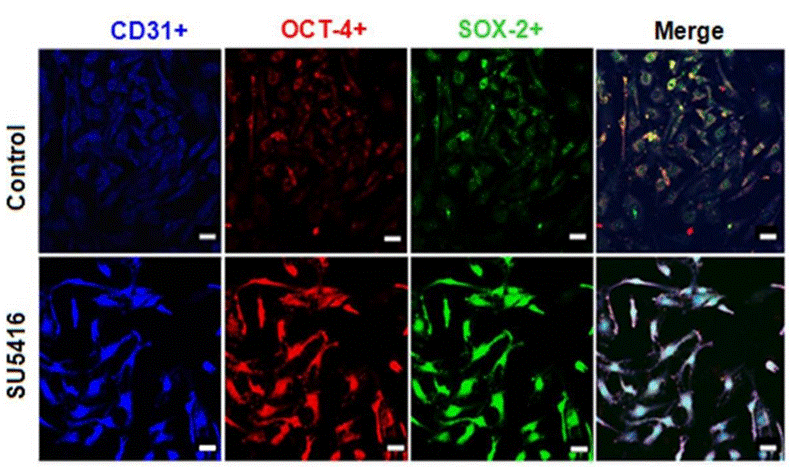
|
25665868 |
Informatie klinische proef
(gegevens van https://clinicaltrials.gov, bijgewerkt op 2024-05-22)
| NCT-nummer | Rekrutering | Aandoeningen | Sponsor/Medewerkers | Startdatum | Fasen |
|---|---|---|---|---|---|
| NCT00006247 | Terminated | Brain and Central Nervous System Tumors |
Pediatric Brain Tumor Consortium|National Cancer Institute (NCI) |
August 2000 | Phase 1 |
| NCT00005642 | Completed | Unspecified Adult Solid Tumor Protocol Specific |
Case Comprehensive Cancer Center|National Cancer Institute (NCI) |
May 2000 | Phase 1 |
| NCT00005647 | Completed | Head and Neck Cancer |
Case Comprehensive Cancer Center|National Cancer Institute (NCI) |
May 2000 | Phase 1 |
Technische ondersteuning
Tel: +1-832-582-8158 Ext:3
Als u nog andere vragen heeft, kunt u een bericht achterlaten.
