uitsluitend voor onderzoeksdoeleinden
AEE788 (NVP-AEE788) EGFR remmer
Cat.Nr.S1486
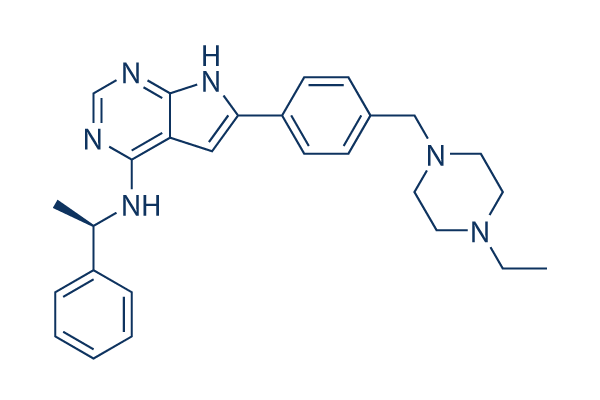
Chemische structuur
Moleculair gewicht: 440.58
Kwaliteitscontrole
| Gerelateerde doelwitten | VEGFR PDGFR FGFR c-Met Src MEK CSF-1R FLT3 HER2 c-Kit |
|---|---|
| Overige EGFR Inhibitoren | Lazertinib (YH25448) Icotinib Hydrochloride Sunvozertinib AG-490 AG-1478 Canertinib (CI-1033) WZ4002 Rociletinib (CO-1686) Poziotinib (NOV120101, HM781-36B) Genistein |
Celkweek, behandeling & werkconcentratie
| Cellijnen | Assaytype | Concentratie | Incubatietijd | Formulering | Activiteitsbeschrijving | PMID |
|---|---|---|---|---|---|---|
| Huh7 | Cytotoxicity assay | Cytotoxicity against human hepatocellular carcinoma cell line (Huh7), CC50=27.83 Μm | ||||
| Jeko B cells | Function assay | 2 h | Inhibition of PI3Kdelta in human Jeko B cells assessed as inhibition of Akt phosphorylation after 2 hrs, IC50=0.017 μM | |||
| Klik om meer experimentele gegevens over de cellijn te bekijken | ||||||
Chemische informatie, Opslag en Stabiliteit
| Moleculair gewicht | 440.58 | Formule | C27H32N6 |
Opslag (Vanaf de ontvangstdatum) | |
|---|---|---|---|---|---|
| CAS-nr. | 497839-62-0 | SDF downloaden | Opslag van stamoplossingen |
|
|
| Synoniemen | N/A | Smiles | CCN1CCN(CC1)CC2=CC=C(C=C2)C3=CC4=C(N3)N=CN=C4NC(C)C5=CC=CC=C5 | ||
Oplosbaarheid
|
In vitro |
DMSO
: 88 mg/mL
(199.73 mM)
Water : Insoluble Ethanol : Insoluble |
Molariteitscalculator
|
In vivo |
|||||
In vivo Formuleringscalculator (Heldere oplossing)
Stap 1: Voer de onderstaande informatie in (Aanbevolen: Een extra dier voor het geval van verlies tijdens het experiment)
Stap 2: Voer de in vivo formulering in (Dit is alleen de calculator, geen formulering. Neem eerst contact met ons op als er geen in vivo formulering is in het gedeelte Oplosbaarheid.)
Berekeningsresultaten:
Werkconcentratie: mg/ml;
Methode voor het bereiden van DMSO-mastervloeistof: mg geneesmiddel vooraf opgelost in μL DMSO ( Concentratie mastervloeistof mg/mL, Neem eerst contact met ons op als de concentratie de DMSO-oplosbaarheid van de partij geneesmiddel overschrijdt. )
Methode voor het bereiden van in vivo formulering: Neem μL DMSO mastervloeistof, voeg vervolgens toeμL PEG300, mengen en helder maken, voeg vervolgens toeμL Tween 80, mengen en helder maken, voeg vervolgens toe μL ddH2O, mengen en helder maken.
Methode voor het bereiden van in vivo formulering: Neem μL DMSO mastervloeistof, voeg vervolgens toe μL Maïsolie, mengen en helder maken.
Opmerking: 1. Zorg ervoor dat de vloeistof helder is voordat u het volgende oplosmiddel toevoegt.
2. Zorg ervoor dat u het/de oplosmiddel(en) in de juiste volgorde toevoegt. U moet ervoor zorgen dat de verkregen oplossing, bij de vorige toevoeging, een heldere oplossing is voordat u verdergaat met het toevoegen van het volgende oplosmiddel. Fysische methoden zoals vortexen, echografie of een warmwaterbad kunnen worden gebruikt om het oplossen te bevorderen.
Werkingsmechanisme
| Targets/IC50/Ki |
EGFR
(Cell-free assay) 2 nM
HER2/ErbB2
(Cell-free assay) 6 nM
c-Abl
(Cell-free assay) 52 nM
FLT1
(Cell-free assay) 59 nM
c-Fms
(Cell-free assay) 60 nM
c-Src
(Cell-free assay) 61 nM
KDR
(Cell-free assay) 77 nM
HER4/ErbB4
(Cell-free assay) 160 nM
|
|---|---|
| In vitro |
AEE788 (NVP-AEE788) remt ook KDR, c-abl, c-Src en Flt-1 met IC50 van 50-80 nM. Het is niet gevoelig voor ErbB-4, PDGFR-
R
, Flt-3, Flt-4, RET en c-Kit en heeft geen remmende werking op Ins-R, IGF-1R, PKC-
R
en PKA. Deze verbinding remt krachtig EGFR-fosforylering in A431-cellen met een IC50 van 11 nM. Het remt ook de fosforylering van KDR in CHO-cellen en erbB2 in BT-474-cellen, zonder enig effect op PDGF-geïnduceerde fosforylering in A31-cellen. Het remt de proliferatie van NCI-H596-, MK-, BT-474- en SK-BR-3-cellen met respectievelijk een IC50 van 78, 56, 49 en 381 nM. Bovendien heeft het de extra eigenschap dat het cellulaire proliferatie remt die wordt aangedreven door EGFR-mutanten, waaronder 32D/EGFR en 32D/EGFRvIII. Het remt verder ook zowel EGF- als VEGF-gedreven HUVEC-proliferatie met respectievelijk een IC50 van 43 en 155 nM. Het remt de fosforylering van EGFR, VEGFR2, Akt en MAPK in menselijke cutane SCC-cellijnen (Colo16-, HaCaT-, SRB1- en SRB12-cellen), wat leidt tot groeiremming en inductie van apoptose. Het remt de fosforylering van EGFR en Akt in HT29-cellen bij 0,2 tot 1,0
R
M. Het remt celproliferatie en voorkomt EGF- en neureguline-geïnduceerde HER1-, HER2- en HER3-activering in medulloblastoomcellijnen. Het vertoont groeiremmende activiteiten in chemosensitieve en chemoresistente medulloblastoomcellen.
|
| Kinase Assay |
Proteïne Kinase Assays
|
|
De in vitro kinase-assays voor AEE788 (NVP-AEE788) worden uitgevoerd in 96-wells platen (30
R
L) bij omgevingstemperatuur gedurende 15–45 min met behulp van de recombinante glutathion S-transferase-gefuseerde kinase-domeinen (4-100 ng, afhankelijk van de specifieke activiteit). [
R
33P]ATP wordt gebruikt als fosfaatdonor en polyGluTyr-(4:1) peptide als acceptor. Met uitzondering van Protein Tyrosine Kinase C-
R
, cycline-afhankelijke kinase 1/cycB en Protein Tyrosine Kinase A zijn protaminesulfaat (200
R
g/mL), histone H1 (100
R
g/mL) en het heptapeptide Leu-Arg-Arg-Ala-Ser-Leu-Gly (bekend als Kemptide Bachem) respectievelijk en worden gebruikt als peptidesubstraten. Assays zijn geoptimaliseerd voor elke kinase met behulp van de volgende ATP-concentraties: 1,0
R
M (c-Kit, c-Met, c-Fms, c-Raf-1 en RET), 2,0
R
M (EGFR, erbB2, ErbB3 en ErbB4), 5,0
R
M (c-abl), 8,0
R
M (Flt-1, Flt-3, Flt-4, Flk, KDR, FGFR-1 en Tek), 10,0
R
M (PDGFR-
R
, Protein Tyrosine Kinase C-
R
en cycline-afhankelijke kinase 1) en 20,0
R
M (c-Src en Protein Tyrosine Kinase A). De reactie wordt beëindigd door toevoeging van 20
R
L 125 mM EDTA. Dertig
R
L (c-abl, c-Src, insuline-achtige groeifactor-1R, RET-Men2A en RET-Men2B) of 40
R
L (alle andere kinasen) van het reactiemengsel wordt overgebracht op Immobilon-polyvinylideenfluoride membraan, voorbevochtigd met 0,5% H3PO4 en gemonteerd op een vacuümverdeelstuk. Vervolgens wordt vacuüm aangelegd en elke put gespoeld met 200
R
L 0,5% H3PO4. Membranen worden verwijderd en vier keer gewassen met 1,0% H3PO4 en eenmaal met ethanol. Gedroogde membranen worden geteld na montage in een Packard TopCount 96-wells frame en met toevoeging van 10
R
L/put Microscint. IC50-waarden (
R
SE) worden berekend door lineaire regressieanalyse van het percentage remming en zijn gemiddelden van ten minste drie bepalingen.
|
|
| In vivo |
AEE788 (NVP-AEE788) produceert een dosisafhankelijke remming van tumorgroei in NCI-H596 of DU145 xenograft-modellen, met slechts geringe veranderingen in lichaamsgewicht. Het induceert tumorregressie met 57% bij 50 mg/kg in het NeuT/erbB2 GeMag-model en remt krachtig EGF-geïnduceerde EGFR-fosforylering in A431-tumoren en erbB2-fosforylering in GeMag-tumoren. Deze verbinding remde dosisafhankelijk VEGF-geïnduceerde angiogenese en remt bFGF-geïnduceerde angiogenese niet. Het onderdrukt de groei van het tumorvolume met 54% in Colo16-xenografts bij 50 mg/kg, wat te wijten is aan de remming van de fosforylering van EGFR, VEGFR, Akt en MAPK. Bij 50 mg/kg remt het ook de groei van tumoren in het coecum en peritoneum (>50%) en vermindert het de incidentie van lymfekliermetastasen tot 70% in HT29-cellen geïmplanteerd in het coecum van naakte muizen, zonder verlies van lichaamsgewicht en duidelijke aanwijzingen voor neovascularisatie. Het verlaagt significant de expressieniveaus van pEGFR en pVEGFR in HT29-coecale tumoren en verandert die van EGF, VEGF, EGFR of VEGFR niet. Gecombineerd met CPT-11 resulteert het in significant kleinere tumoren en volledige remming van lymfekliermetastasen. Deze verbinding remt de groei van Daoy-, DaoyPt- en DaoyHER2-xenografts met respectievelijk 51%, 45% en 72%. Het zou LBH589-gemedieerde generatie van reactieve zuurstofsoorten in K562-tumorcellen kunnen bevorderen, wat op zijn beurt apoptose verhoogt.
|
Referenties |
|
Informatie klinische proef
(gegevens van https://clinicaltrials.gov, bijgewerkt op 2024-05-22)
| NCT-nummer | Rekrutering | Aandoeningen | Sponsor/Medewerkers | Startdatum | Fasen |
|---|---|---|---|---|---|
| NCT00107237 | Completed | Brain and Central Nervous System Tumors |
Novartis Pharmaceuticals|Novartis |
October 2003 | Phase 1|Phase 2 |
| NCT00118456 | Completed | Cancer |
Novartis Pharmaceuticals|Novartis |
July 2003 | Phase 1 |
Technische ondersteuning
Tel: +1-832-582-8158 Ext:3
Als u nog andere vragen heeft, kunt u een bericht achterlaten.
