réservé à la recherche
Sorafenib Tosylate (BAY 43-9006) Inhibiteur de Raf/VEGFR
N° Cat.S1040
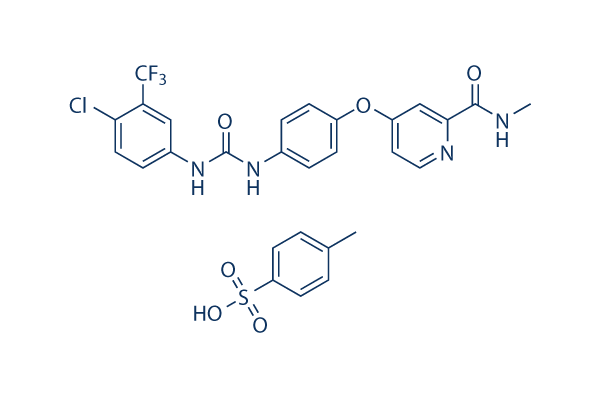
Structure chimique
Poids moléculaire: 637.03
Contrôle qualité
Produits Souvent Utilisés Avec Sorafenib Tosylate (BAY 43-9006)
| Cibles apparentées | ERK p38 MAPK JNK MEK Ras KRas S6 Kinase MAP4K TAK1 Mixed Lineage Kinase |
|---|---|
| Autre Raf Inhibiteurs | LY3009120 Exarafenib (KIN-2787) GDC-0879 Avutometinib (Ro5126766, CH5126766) PLX-4720 AZ 628 SB590885 TAK-632 GW5074 RAF265 (CHIR-265) |
Culture cellulaire, traitement et concentration de travail
| Lignées cellulaires | Type dessai | Concentration | Temps dincubation | Formulation | Description de lactivité | PMID |
|---|---|---|---|---|---|---|
| MDA-MB-435 | Growth Inhibition Assay | 48 h | GI50=2 μM | 22560627 | ||
| UACC257 | Growth Inhibition Assay | 48 h | GI50=2 μM | 22560627 | ||
| MCF7 | Growth Inhibition Assay | 48 h | GI50=2.5 μM | 22560627 | ||
| EKVX | Growth Inhibition Assay | 48 h | GI50=2.5 μM | 22560627 | ||
| HT-29 | Growth Inhibition Assay | 48 h | GI50=2.5 μM | 22560627 | ||
| SNB19 | Growth Inhibition Assay | 48 h | GI50=3.2 μM | 22560627 | ||
| OVCAR3 | Growth Inhibition Assay | 48 h | GI50=3.2 μM | 22560627 | ||
| CAKI-1 | Growth Inhibition Assay | 48 h | GI50=3.2 μM | 22560627 | ||
| SW620 | Growth Inhibition Assay | 48 h | GI50=3.2 μM | 22560627 | ||
| TK10 | Growth Inhibition Assay | 48 h | GI50=5 μM | 22560627 | ||
| endothelial precursor cells | Function assay | Inhibition of endothelial cord area formation in endothelial precursor cells by CD31 cord area detection based phenotypic drug discovery based assay, IC50 = 0.00421 μM. | 22409666 | |||
| Sf9 | Function assay | Inhibition of GST-tagged recombinant human VEGFR2 expressed in Sf9 cells by radiometric assay, IC50 = 0.0125 μM. | 24368209 | |||
| endothelial precursor cells/ADSC cells | Toxicity assay | Toxicity in endothelial precursor cells co-cultured with stromal precursor ADSC cells by total nuclei count detection based phenotypic drug discovery based assay, EC50 = 5.46 μM. | 22409666 | |||
| endothelial precursor cells | Function assay | Inhibition of cell migration in endothelial precursor cells by Oris cell migration kit based phenotypic drug discovery based assay, IC50 = 16.7 μM. | 22409666 | |||
| RD | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for RD cells | 29435139 | |||
| SK-N-SH | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for SK-N-SH cells | 29435139 | |||
| OHS-50 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for OHS-50 cells | 29435139 | |||
| Cliquez pour voir plus de données expérimentales sur les lignées cellulaires | ||||||
Informations chimiques, stockage et stabilité
| Poids moléculaire | 637.03 | Formule | C21H16ClF3N4O3.C7H8O3S |
Stockage (À partir de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 475207-59-1 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | BAY 43-9006 tosylate,NSC-724772 tosylate | Smiles | CC1=CC=C(C=C1)S(=O)(=O)O.CNC(=O)C1=NC=CC(=C1)OC2=CC=C(C=C2)NC(=O)NC3=CC(=C(C=C3)Cl)C(F)(F)F | ||
Solubilité
|
In vitro |
DMSO
: 127 mg/mL
(199.36 mM)
Water : 0.01 mg/mL Ethanol : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Entrez les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Entrez la formulation in vivo (Ceci nest que le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuiteμL PEG300, mélanger et clarifier, ajouter ensuiteμL Tween 80, mélanger et clarifier, ajouter ensuite μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuite μL Huile de maïs, mélanger et clarifier.
Remarque : 1. Assurez-vous que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue lors de lajout précédent est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
Raf-1
(Cell-free assay) 6 nM
VEGFR2/Flk1
(Cell-free assay) 15 nM
B-Raf
(Cell-free assay) 22 nM
B-Raf (V599E)
(Cell-free assay) 38 nM
PDGFRβ
(Cell-free assay) 57 nM
mPDGFRβ
(Cell-free assay) 57 nM
FLT3
(Cell-free assay) 58 nM
c-Kit
(Cell-free assay) 68 nM
VEGFR2
(Cell-free assay) 90 nM
FGFR1
(Cell-free assay) 580 nM
|
|---|---|
| In vitro |
Le tosylate de Sorafenib inhibe l'activité de B-Raf de type sauvage et de type mutant V599E avec des IC50 de 22 nM et 38 nM, respectivement. Ce composé inhibe également puissamment mVEGFR2 (Flk-1), mVEGFR3, mPDGFRβ, Flt3 et c-Kit avec des IC50 de 15 nM, 20 nM, 57 nM, 58 nM et 68 nM, respectivement. Il inhibe faiblement FGFR-1 avec une IC50 de 580 nM. Ce produit chimique n'est pas actif contre ERK-1, MEK-1, EGFR, HER-2, IGFR-1, c-Met, PKB, PKA, cdk1/cyclinB, PKCα, PKCγ et pim-1. Il inhibe de manière significative la phosphorylation de VEGFR2 dans les cellules NIH 3T3 avec une IC50 de 30 nM et la phosphorylation de Flt-3 dans les cellules HEK-293 avec une IC50 de 20 nM. Il bloque puissamment la phosphorylation de MEK 1/2 et ERK 1/2 dans la plupart des lignées cellulaires mais pas dans les cellules A549 ou H460, tout en n'ayant aucun effet sur l'inhibition de la voie PKB. Il inhibe la prolifération des cellules HAoSMC et MDA-MB-231 avec des IC50 de 0,28 μM et 2,6 μM, respectivement. En plus de l'inhibition de la voie de signalisation RAF/MEK/ERK, il inhibe significativement la phosphorylation de eIF4E et régule à la baisse les niveaux de Mcl-1 dans les cellules de carcinome hépatocellulaire (HCC) de manière indépendante de MEK/ERK. Il inhibe la prolifération des cellules PLC/PRF/5 et HepG2 avec des IC50 de 6,3 μM et 4,5 μM, respectivement, et entraîne une induction significative de l'apoptosis. |
| Kinase Assay |
Tests biochimiques
|
|
Les baculovirus recombinants exprimant Raf-1 (résidus 305–648) et B-Raf (résidus 409–765) sont purifiés sous forme de protéines de fusion. Le MEK-1 humain pleine longueur est généré par PCR et purifié sous forme de protéine de fusion à partir de lysats d'Escherichia coli. Sorafenib tosylate est ajouté à un mélange de Raf-1 (80 ng), ou B-Raf (80 ng) avec MEK-1 (1 μg) dans un tampon d'essai [20 mM Tris (pH 8.2), 100 mM NaCl, 5 mM MgCl2, et 0,15% β-mercaptoéthanol] à une concentration finale de 1% de DMSO. L'essai de la kinase Raf (volume final de 50 μL) est initié par l'ajout de 25 μL de 10 μM γ[33P]ATP (400 Ci/mol) et incubé à 32 °C pendant 25 minutes. Le MEK-1 phosphorylé est récolté par filtration sur un tapis de phosphocellulose, et 1% d'acide phosphorique est utilisé pour éliminer la radioactivité non liée. Après séchage par chauffage micro-ondes, un compteur à plaque β est utilisé pour quantifier la radioactivité liée au filtre. Le domaine kinase de VEGFR2 (KDR) humain est exprimé et purifié à partir de lysats de Sf9. Des essais de transfert d'énergie par fluorescence résolue dans le temps pour VEGFR2 sont effectués dans des plaques opaques à 96 puits au format de transfert d'énergie par fluorescence résolue dans le temps. Les conditions de réaction finales sont les suivantes : 1 à 10 μM ATP, 25 nM poly GT-biotine, 2 nM anticorps phospho (p)-Tyr marqué à l'europium (PY20), 10 nM APC, 1 à 7 nM domaine kinase cytoplasmique à des concentrations finales de 1% de DMSO, 50 mM HEPES (pH 7.5), 10 mM MgCl2, 0,1 mM EDTA, 0,015% Brij-35, 0,1 mg/mL BSA, et 0,1% β-mercaptoéthanol. Les volumes de réaction sont de 100 μL et sont initiés par l'ajout d'enzyme. Les plaques sont lues à la fois à 615 et 665 nM sur un compteur Multilabel Perkin-Elmer VictorV environ 1,5 à 2,0 heures après l'initiation de la réaction. Le signal est calculé comme un rapport : (665 nm/615 nM) × 10 000 pour chaque puits. Pour la génération de l'IC50, ce composé est ajouté avant l'initiation de l'enzyme. Une plaque de stock 50 fois est préparée avec ce produit chimique dilué en série au 1:3 dans une solution de 50% de DMSO/50% d'eau distillée. Les concentrations finales de ce composé varient de 10 μM à 4,56 nM dans 1% de DMSO.
|
|
| In vivo |
L'administration orale de Sorafenib tosylate (~60 mg/kg) démontre une activité antitumorale à large spectre et dose-dépendante contre une variété de modèles de xénogreffes tumorales humaines, y compris MDA-MB-231, Colo-205, HT-29, DLD-1, NCI-H460 et A549, sans preuve de toxicité. En association avec l'efficacité antitumorale, ce traitement par composé inhibe puissamment la phosphorylation de MEK 1/2 et les niveaux de pERK 1/2 dans les xénogreffes HT-29 et MDA-MB-231, mais pas dans les xénogreffes Colo-205, et supprime significativement la surface des microvaisseaux tumoraux (MVA) et la densité des microvaisseaux (MVD) dans les xénogreffes tumorales MDA MB-231, HT-29 et Colo-205. Ce traitement par composé produit une inhibition de la croissance dose-dépendante des xénogreffes tumorales PLC/PRF/5 chez les souris SCID avec des TGI de 49% et 78% à 10 mg/kg et 30 mg/kg, respectivement, ce qui est cohérent avec l'inhibition de la phosphorylation d'ERK et d'eIF4E, la réduction de la surface des microvaisseaux et l'induction de l'apoptosis des cellules tumorales. |
Références |
|
Applications
| Méthodes | Biomarqueurs | Images | PMID |
|---|---|---|---|
| Western blot | LC3-I / LC-3II / ATG5 p-STAT3 / STAT3/ Mcl-1 β-catenin / Survivin / Mcl-1 / PTMA pERK / ERK p-PKM2(Y105) / PMK2 / Caspase-9 RET(pY1016) / VEGFR2(pY1214) / MEK1(pT292) / ERK(pY204) Cyclin D1 |
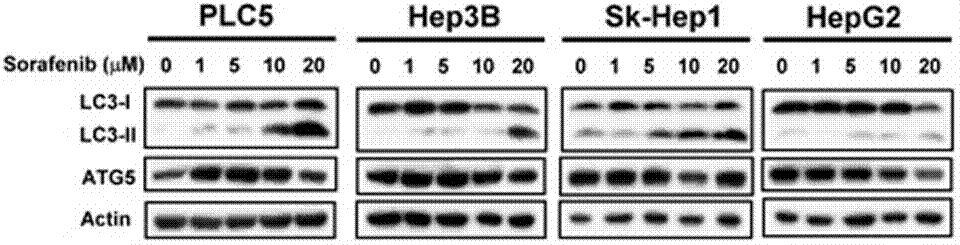
|
23392173 |
| Immunofluorescence | p65 cytochrome c |
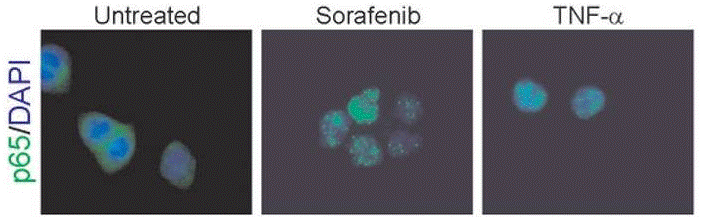
|
22286758 |
| Growth inhibition assay | Cell viability |
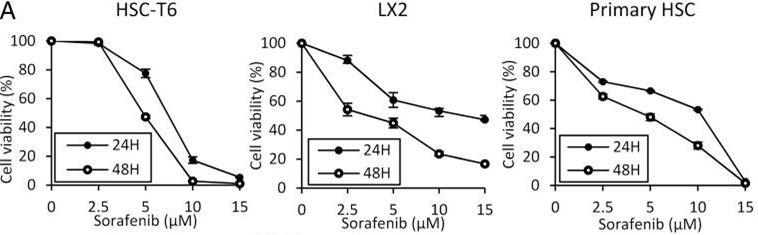
|
26039995 |
| ELISA | TGF-beta / CD206 Caspase-9 / Caspase-3 |
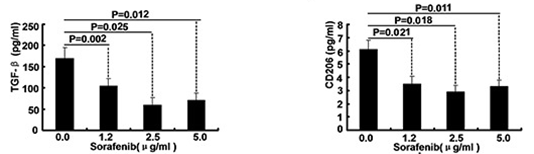
|
26158762 |
Informations sur lessai clinique
(données de https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Sponsor/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT05068752 | Recruiting | Pancreas Cancer |
HonorHealth Research Institute|Bayer|Genentech Inc. |
October 28 2021 | Phase 2 |
| NCT04763408 | Active not recruiting | Carcinoma Hepatocellular |
Eisai Inc. |
April 9 2021 | -- |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
