Données techniques
| Formule | C21H16ClF3N4O3.C7H8O3S |
||||||||||||||
| Poids moléculaire | 637.03 | N° CAS | 475207-59-1 | ||||||||||||
| Solubilité (25°C)* | In vitro | DMSO | 127 mg/mL (199.36 mM) | ||||||||||||
| Water | 0.01 mg/mL (0.01 mM) | ||||||||||||||
| Ethanol | Insoluble | ||||||||||||||
| In Vivo (Ajoutez les solvants au produit individuellement et dans lordre.) |
|
||||||||||||||
|
* <1 mg/ml signifie légèrement soluble ou insoluble. * Veuillez noter que Selleck teste la solubilité de tous les composés en interne, et la solubilité réelle peut différer légèrement des valeurs publiées. Ceci est normal et est dû à de légères variations dun lot à lautre. * Expédition à température ambiante (les tests de stabilité montrent que ce produit peut être expédié sans aucune mesure de refroidissement.) |
|||||||||||||||
Préparation des solutions mères
Activité biologique
| Description | Sorafenib Tosylate est un inhibiteur multi-kinase de Raf-1 et B-Raf avec un IC50 de 6 nM et 22 nM dans des essais acellulaires, respectivement. Sorafenib Tosylate inhibe VEGFR-2, VEGFR-3, PDGFR-β, Flt-3 et c-KIT avec un IC50 de 90 nM, 20 nM, 57 nM, 59 nM et 68 nM, respectivement. Sorafenib Tosylate induit l'autophagy et l'apoptosis et active la ferroptosis avec une activité anti-tumorale. | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Cibles |
|
|||||||||||
| In vitro | Le tosylate de Sorafenib inhibe l'activité de B-Raf de type sauvage et de type mutant V599E avec des IC50 de 22 nM et 38 nM, respectivement. Ce composé inhibe également puissamment mVEGFR2 (Flk-1), mVEGFR3, mPDGFRβ, Flt3 et c-Kit avec des IC50 de 15 nM, 20 nM, 57 nM, 58 nM et 68 nM, respectivement. Il inhibe faiblement FGFR-1 avec une IC50 de 580 nM. Ce produit chimique n'est pas actif contre ERK-1, MEK-1, EGFR, HER-2, IGFR-1, c-Met, PKB, PKA, cdk1/cyclinB, PKCα, PKCγ et pim-1. Il inhibe de manière significative la phosphorylation de VEGFR2 dans les cellules NIH 3T3 avec une IC50 de 30 nM et la phosphorylation de Flt-3 dans les cellules HEK-293 avec une IC50 de 20 nM. Il bloque puissamment la phosphorylation de MEK 1/2 et ERK 1/2 dans la plupart des lignées cellulaires mais pas dans les cellules A549 ou H460, tout en n'ayant aucun effet sur l'inhibition de la voie PKB. Il inhibe la prolifération des cellules HAoSMC et MDA-MB-231 avec des IC50 de 0,28 μM et 2,6 μM, respectivement. En plus de l'inhibition de la voie de signalisation RAF/MEK/ERK, il inhibe significativement la phosphorylation de eIF4E et régule à la baisse les niveaux de Mcl-1 dans les cellules de carcinome hépatocellulaire (HCC) de manière indépendante de MEK/ERK. Il inhibe la prolifération des cellules PLC/PRF/5 et HepG2 avec des IC50 de 6,3 μM et 4,5 μM, respectivement, et entraîne une induction significative de l'apoptosis. |
|||||||||||
| In Vivo | L'administration orale de Sorafenib tosylate (~60 mg/kg) démontre une activité antitumorale à large spectre et dose-dépendante contre une variété de modèles de xénogreffes tumorales humaines, y compris MDA-MB-231, Colo-205, HT-29, DLD-1, NCI-H460 et A549, sans preuve de toxicité. En association avec l'efficacité antitumorale, ce traitement par composé inhibe puissamment la phosphorylation de MEK 1/2 et les niveaux de pERK 1/2 dans les xénogreffes HT-29 et MDA-MB-231, mais pas dans les xénogreffes Colo-205, et supprime significativement la surface des microvaisseaux tumoraux (MVA) et la densité des microvaisseaux (MVD) dans les xénogreffes tumorales MDA MB-231, HT-29 et Colo-205. Ce traitement par composé produit une inhibition de la croissance dose-dépendante des xénogreffes tumorales PLC/PRF/5 chez les souris SCID avec des TGI de 49% et 78% à 10 mg/kg et 30 mg/kg, respectivement, ce qui est cohérent avec l'inhibition de la phosphorylation d'ERK et d'eIF4E, la réduction de la surface des microvaisseaux et l'induction de l'apoptosis des cellules tumorales. |
Protocole (de référence)
| Test kinase : |
|
|---|---|
| Test cellulaire : |
|
| Étude animale : |
|
Références
|
Validation du produit par le client
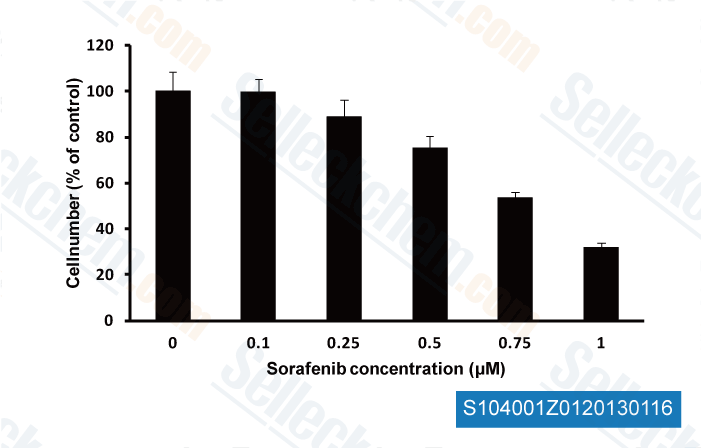
-
, 2013 , Christina W Yde/CDM Danish Cancer Society Research Center Denmark
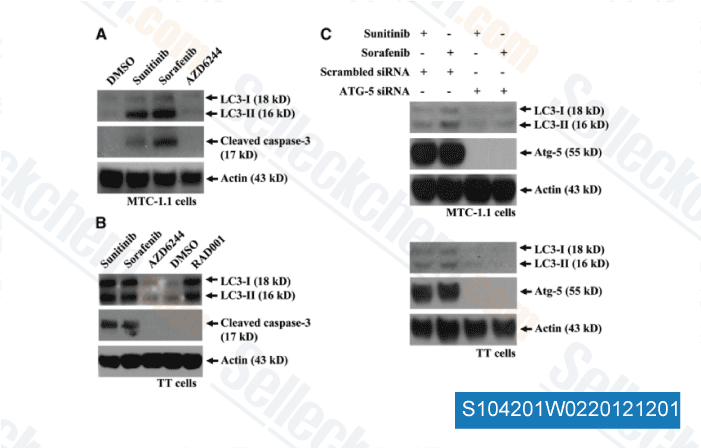
-
Données de [ Surgery , 2012 , 152(6), 1142-9 ]
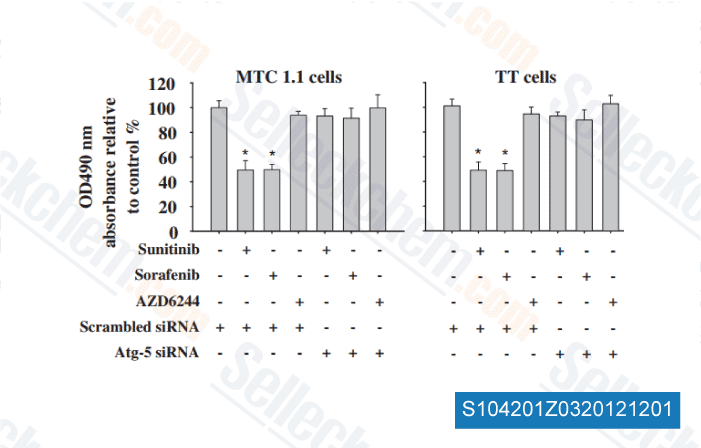
-
Données de [ Surgery , 2012 , 152(6), 1142-9 ]
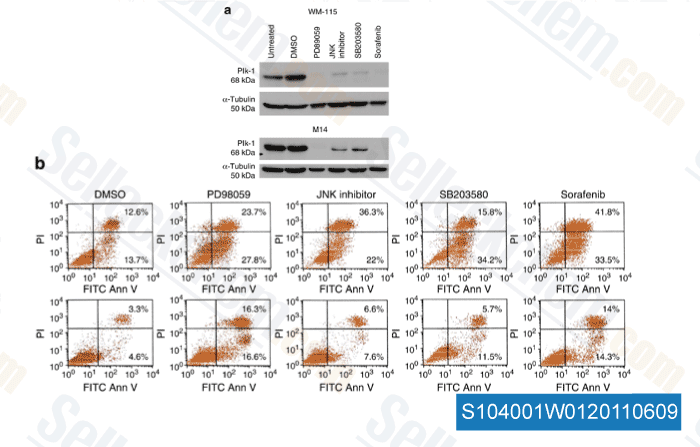
-
Données de [ J Invest Dermatol , 2011 , 131, 1886–1895 ]
De Selleck Sorafenib Tosylate (BAY 43-9006) A été cité par 274 Publications
| Inhibiting SSBP1 enhances ferroptosis and improves the effectiveness of sorafenib treatment for liver cancer [ Int J Oncol, 2025, 67(3)72] | PubMed: 40747667 |
| Tumour-selective activity of RAS-GTP inhibition in pancreatic cancer [ Nature, 2024, 629(8013):927-936] | PubMed: 38588697 |
| Targeting NG2 relieves the resistance of BRAF-mutant thyroid cancer cells to BRAF inhibitors [ Cell Mol Life Sci, 2024, 81(1):238] | PubMed: 38795180 |
| Mitochondrial GCN5L1 acts as a novel regulator for iron homeostasis to promote sorafenib sensitivity in hepatocellular carcinoma [ J Transl Med, 2024, 22(1):593] | PubMed: 38918793 |
| IL-22 signaling promotes sorafenib resistance in hepatocellular carcinoma via STAT3/CD155 signaling axis [ Front Immunol, 2024, 15:1373321] | PubMed: 38596684 |
| Patient-derived rhabdomyosarcoma cells recapitulate the genetic and transcriptomic landscapes of primary tumors [ iScience, 2024, 27(10):110862] | PubMed: 39319271 |
| EZH2 suppresses ferroptosis in hepatocellular carcinoma and reduces sorafenib sensitivity through epigenetic regulation of TFR2 [ Cancer Sci, 2024, 115(7):2220-2234] | PubMed: 38623968 |
| Upregulation of LHPP by saRNA inhibited hepatocellular cancer cell proliferation and xenograft tumor growth [ PLoS One, 2024, 19(5):e0299522] | PubMed: 38696452 |
| Gravitational and mechanical forces drive mitochondrial translation [ bioRxiv, 2024, 10.1101/2023.01.18.524628] | PubMed: none |
| Arginine reprograms metabolism in liver cancer via RBM39 [ Cell, 2023, 186(23):5068-5083.e23] | PubMed: 37804830 |
POLITIQUE DE RETOUR
La politique de retour inconditionnelle de Selleck Chemical garantit une expérience dachat en ligne fluide à nos clients. Si vous nêtes en aucun cas satisfait de votre achat, vous pouvez retourner tout article dans les 7 jours suivant sa réception. En cas de problèmes de qualité du produit, quil sagisse de problèmes liés au protocole ou au produit, vous pouvez retourner tout article dans les 365 jours suivant la date dachat initiale. Veuillez suivre les instructions ci-dessous lors du retour des produits.
EXPÉDITION ET STOCKAGE
Les produits Selleck sont transportés à température ambiante. Si vous recevez le produit à température ambiante, soyez assuré que le service dinspection de la qualité de Selleck a mené des expériences pour vérifier que le placement à température normale pendant un mois naffectera pas lactivité biologique des produits en poudre. Après réception, veuillez stocker le produit conformément aux exigences décrites dans la fiche technique. La plupart des produits Selleck sont stables dans les conditions recommandées.
NON DESTINÉ À UN USAGE HUMAIN, VÉTÉRINAIRE DIAGNOSTIQUE OU THÉRAPEUTIQUE.
