réservé à la recherche
AG-490 EGFR inhibiteur
N° Cat.S1143
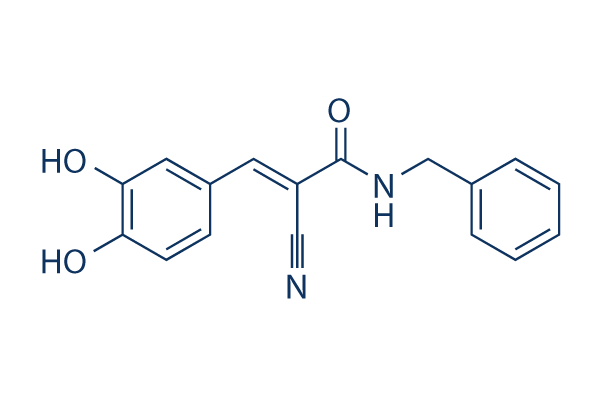
Structure chimique
Poids moléculaire: 294.30
Contrôle qualité
| Cibles apparentées | VEGFR PDGFR FGFR c-Met Src MEK CSF-1R FLT3 HER2 c-Kit |
|---|---|
| Autre EGFR Inhibiteurs | Lazertinib (YH25448) Icotinib Hydrochloride Sunvozertinib AG-1478 Canertinib (CI-1033) WZ4002 Rociletinib (CO-1686) Poziotinib (NOV120101, HM781-36B) Genistein Allitinib tosylate |
Culture cellulaire, traitement et concentration de travail
| Lignées cellulaires | Type dessai | Concentration | Temps dincubation | Formulation | Description de lactivité | PMID |
|---|---|---|---|---|---|---|
| BC3 | Function Assay | 100 µM | 24 h | mediates PEL cell apoptosis | ||
| BCBL1 | Function Assay | 100 µM | 24 h | mediates PEL cell apoptosis | ||
| BC3 | Function Assay | 100 µM | 24 h | mediates de-phosphorylation of STAT3 correlated with HSP70 and HSF1 reduction | ||
| BCBL1 | Function Assay | 100 µM | 24 h | mediates de-phosphorylation of STAT3 correlated with HSP70 and HSF2 reduction | ||
| BC3 | Function Assay | 100 µM | 24 h | induces a complete autophagic flux | ||
| BCBL1 | Function Assay | 100 µM | 24 h | induces a complete autophagic flux | ||
| SK-MEL-28 | Function Assay | 50/100 µM | 48 h | DMSO | reduces anoikis resistance | |
| MeWo | Function Assay | 50/100 µM | 48 h | DMSO | reduces anoikis resistance | |
| SK-MEL-5 | Function Assay | 50/100 µM | 48 h | DMSO | reduces anoikis resistance | |
| SK-MEL-2 | Function Assay | 50/100 µM | 48 h | DMSO | reduces anoikis resistance | |
| B16-F0 | Function Assay | 50/100 µM | 48 h | DMSO | reduces anoikis resistance | |
| TRPM2/HEK | Function Assay | 0.1–25 µM | 15 min | DMSO | reduces H2O2-induced Ca2+increase in a concentration-dependent manner, and the IC50 value was 1.7 µM | |
| U937 | Function Assay | 0.1–25 µM | 15 min | DMSO | reduces H2O2-induced Ca2+increase in a concentration-dependent manner, and the IC50 value was 0.4 µM | |
| TRPM2/HEK | Function Assay | 10 µM | 40 min | DMSO | reduces TRPM2 activation even at high concentrations of H2O2 | |
| GL37 | Cell Viability Assay | 0-10 µM | 48 h | suppresses La expression | ||
| NRK-52E | Function Assay | 1 µM | 10 min | blocks the stimulatory effect of Ang II on Pax-2 expression | ||
| NRK-52E | Function Assay | 1 µM | 10 min | blocks Ang II induced CD24 expression | ||
| HSC | Function Assay | 20 μM | 1 h | abrogates the differential effects of leptin or AGEs | ||
| EJ | Growth Inhibition Assay | 50/80 μM | 24/48/72 h | inhibits cell growth in both time and dose dependent manner | ||
| EJ | Growth Inhibition Assay | 50/80 μM | 48 h | causes S-phase arrest | ||
| EJ | Function Assay | 50/80 μM | 48 h | downregulates c-Myc, cyclinD1, survivin and VEGF expressions | ||
| HepG2 | Function Assay | 50-500 μM | 60 min | inhibits the IL-6-induced phosphorylation of STAT1 (Tyr705) and STAT3 (Tyr705) in a dose-dependent manner | ||
| SGC7901 | Cell Viability Assay | 0-100 μM | 24/48/72 h | causes a significant reduction in cell viability dose-dependently but not time-dependently | ||
| AGS | Cell Viability Assay | 0-100 μM | 24/48/72 h | causes a significant reduction in cell viability dose-dependently but not time-dependently | ||
| SGC7901 | Function Assay | 50 μM | 24/48/72 h | the levels of pJAK2 began to decline at 24 hr, and rebounded at 72 hr | ||
| AGS | Function Assay | 50 μM | 24/48/72 h | the levels of pJAK2 began to decline at 24 hr, and rebounded at 72 hr | ||
| SGC7901 | Function Assay | 50 μM | 24/48/72 h | the cytoplasmic localization of pJAK2 (JAK2 phosphorylated at residues Tyr1007 and Tyr1008) decreased after AG490 treatment for 24 and 48 hr, but started to rebound at 72 hr | ||
| AGS | Function Assay | 50 μM | 24/48/72 h | the cytoplasmic localization of pJAK2 (JAK2 phosphorylated at residues Tyr1007 and Tyr1008) decreased after AG490 treatment for 24 and 48 hr, but started to rebound at 72 hr | ||
| MC3T3-E1 | Function Assay | 50 μM | 4 h | inhibits HSE-induced BMP7 and GHR protein expression | ||
| 7TD1-DXM | Growth Inhibition Assay | 10 μM | 72 h | DMSO | inhibits cell growth | |
| 7TD1-WD-90 | Growth Inhibition Assay | 10 μM | 72 h | DMSO | inhibits cell growth | |
| 7TD1-DXM | Apoptosis Assay | 50 μM | 48 h | DMSO | induces apoptosis | |
| 7TD1-WD-90 | Apoptosis Assay | 50 μM | 48 h | DMSO | induces apoptosis | |
| 7TD1-WD-90 | Function Assay | 50 μM | 6 h | DMSO | significantly inhibits the phosphorylation of JAK2 and phosphorylation of STAT3 | |
| HepG2 | Function Assay | 100 μM | 12/24 h | inhibits STAT3 tyrosine phosphorylation | ||
| RAW264.7 | Function Assay | 50 μM | 24/48 h | suppresses RANKL-induced osteoclastogenesis | ||
| RAW264.7 | Growth Inhibition Assay | 0-50 μM | 48 h | inhibits cell growth dose-dependently | ||
| RAW264.7 | Growth Inhibition Assay | 0-50 μM | 48 h | causes an arrest of RAW264.7 cells at the G0/G1 phase of the cell cycle | ||
| RAW264.7 | Function Assay | 50 μM | 24/48 h | inhibits RANKL-induced NFATc1 expression and phosphorylation of Ser727STAT3 | ||
| A549 | Function Assay | 20/40 μM | 20 h | 20 μM AG490 suppresses the radiation-induced invasion of A549 cells | ||
| A549 | Function Assay | 10/20/40 μM | 24 h | suppresses the radiation-induced elevation of VEGF | ||
| HUVECs | Cell Viability Assay | 20 µM | 4 h | attenuates H2O2-induced cell shrinkage and improved the attachment rate of the cells | ||
| HUVECs | Apoptosis Assay | 20 µM | 4 h | significantly decreases the cell apoptotic index | ||
| BV-2 | Function Assay | 20 µM | 16 h | inhibits LPS-induced STAT1 phosphorylation with almost completely diminished iNOS expression | ||
| NRK-52E | Function Assay | 5 μM | 30 min | attenuates Ang-(1–7)-inhibited TGF-β1 mRNA at 16 h | ||
| SW620 | Function Assay | 20 µM | 1/6 h | inhibits p-STAT3 activation | ||
| RPE | Function Assay | 30 µM | 3 h | inhibits the induction of p-STAT3 expression | ||
| SW1116 | Function Assay | 100 µM | 24/48/72 h | decreases the expression of JAK2 and pJAK2 time-dependently | ||
| HT29 | Function Assay | 100 µM | 24/48/72 h | decreases the expression of JAK2 and pJAK2 time-dependently | ||
| SW1116 | Function Assay | 100 µM | 24/48/72 h | decreases the pSTAT3 levels in a time-dependent manner | ||
| HT29 | Function Assay | 100 µM | 24/48/72 h | decreases the pSTAT3 levels in a time-dependent manner | ||
| ARPE-19 | Function Assay | 5 μM | 30 min | inhibits JAK2 phosphorilation | ||
| HSC-T6 | Apoptosis Assay | 10 μM | 2 h | inhibits the apoptosis of HSC-T6 cells induced by CDE | ||
| HSC-T6 | Function Assay | 10 μM | 2 h | inhibits the expressions of pY-STAT1 and Bad induced by CDE | ||
| Hep-2 | Growth Inhibition Assay | 25-100 μM | 24/48/72 h | inhibits cell growth in both time and dose dependent manner | ||
| Hep-2 | Apoptosis Assay | 50 μM | 24/48/72 h | induces cell apoptosis time dependently | ||
| Hep-2 | Function Assay | 50 μM | 24/48/72 h | inhibits G1 to S cell cycle transition and induces G1 cell cycle arrest | ||
| Hep-2 | Function Assay | 50 μM | 24/48/72 h | downregulates the STAT3, p-STAT3 and survivin protein levels | ||
| KF8 | Function Assay | 10 μM | 1 h | DMSO | inhibits IL-33-induced NF-κB activation | |
| KF8 | Function Assay | 10 μM | 1 h | DMSO | inhibits IL-33-induced IκBα degradation and NF-κB activation | |
| HEL | Function Assay | 100 μM | 12-72 h | inhibits the level of p-JAK2, JAK2 | ||
| HEL | Growth Inhibition Assay | 100 μM | 0-5 d | reduces growth of JAK2V617F-expressing HEL cells | ||
| A-172 | Function Assay | 50/100 μM | 48 h | reduces the levels of constitutively activated STAT3 in a time-dependent and dose-dependent fashion | ||
| MZ-18 | Function Assay | 50/100 μM | 48 h | reduces the levels of constitutively activated STAT3 in a time-dependent and dose-dependent fashion | ||
| MZ-54 | Function Assay | 50/100 μM | 48 h | reduces the levels of constitutively activated STAT3 in a time-dependent and dose-dependent fashion | ||
| MZ-256 | Function Assay | 50/100 μM | 48 h | reduces the levels of constitutively activated STAT3 in a time-dependent and dose-dependent fashion | ||
| MZ-304 | Function Assay | 50/100 μM | 48 h | reduces the levels of constitutively activated STAT3 in a time-dependent and dose-dependent fashion | ||
| A-172 | Growth Inhibition Assay | 50/100 μM | 48 h | leads to a statistically significant reduction of cell proliferation over a time period of 48 h | ||
| MZ-18 | Growth Inhibition Assay | 50/100 μM | 48 h | leads to a statistically significant reduction of cell proliferation over a time period of 48 h | ||
| MZ-54 | Growth Inhibition Assay | 50/100 μM | 48 h | leads to a statistically significant reduction of cell proliferation over a time period of 48 h | ||
| MZ-256 | Growth Inhibition Assay | 50/100 μM | 48 h | leads to a statistically significant reduction of cell proliferation over a time period of 48 h | ||
| MZ-304 | Growth Inhibition Assay | 50/100 μM | 48 h | leads to a statistically significant reduction of cell proliferation over a time period of 48 h | ||
| A-172 | Function Assay | 50/100 μM | 48 h | inhibits migration | ||
| MZ-18 | Function Assay | 50/100 μM | 48 h | inhibits migration | ||
| MZ-54 | Function Assay | 50/100 μM | 48 h | inhibits migration | ||
| MZ-256 | Function Assay | 50/100 μM | 48 h | inhibits migration | ||
| MZ-304 | Function Assay | 50/100 μM | 48 h | inhibits migration | ||
| A-172 | Function Assay | 100 μM | 48 h | inhibits invasion | ||
| MZ-18 | Function Assay | 100 μM | 48 h | inhibits invasion | ||
| MZ-54 | Function Assay | 100 μM | 48 h | inhibits invasion | ||
| MZ-256 | Function Assay | 100 μM | 48 h | inhibits invasion | ||
| MZ-304 | Function Assay | 100 μM | 48 h | inhibits invasion | ||
| A-172 | Function Assay | 50/100 μM | 48 h | reduces transcription of MMP genes and reduces enzymatic activity of MMPs | ||
| MZ-18 | Function Assay | 50/100 μM | 48 h | reduces transcription of MMP genes and reduces enzymatic activity of MMPs | ||
| MZ-54 | Function Assay | 50/100 μM | 48 h | reduces transcription of MMP genes and reduces enzymatic activity of MMPs | ||
| MZ-256 | Function Assay | 50/100 μM | 48 h | reduces transcription of MMP genes and reduces enzymatic activity of MMPs | ||
| MZ-304 | Function Assay | 50/100 μM | 48 h | reduces transcription of MMP genes and reduces enzymatic activity of MMPs | ||
| SW1990 | Growth Inhibition Assay | 20 μM | 24/48/72 h | inhibits cell growth time dependently | ||
| SW1990 | Function Assay | 20 μM | 24 h | decreases the expression of MMP-2 and VEGF mRNAs | ||
| SW1990 | Function Assay | 20 μM | 24 h | decreases the intensity of p-Stat3 expression | ||
| SW1990 | Invasion Assay | 20 μM | 24 h | reduces invasion of SW1990 cells | ||
| THP1 | Function Assay | 10 uM | 30 min | inhibits STAT3 tyrosine phosphorylation by over 60% | ||
| BMMC | Function Assay | 0-10 μM | 15 min | inhibits LTC4 release in a dose-dependent fashion with near complete inhibition at concentrations ⩾10 μM | ||
| A549 | Function Assay | 15 μm | 1 h | inhibits the phosphorylation of STAT1 on tyrosine 701 was detected 15 min after SPE B treatment | ||
| OVCAR-3 | Function Assay | 10 uM | 1 h | inhibits LPA-induced STAT3 phosphorylation | ||
| PA-1 | Function Assay | 10 uM | 1 h | inhibits LPA-induced STAT3 phosphorylation | ||
| OVCAR-3 | Function Assay | 10 uM | 1 h | inhibits LPA-induced ovarian cancer cell motility | ||
| PA-1 | Function Assay | 10 uM | 1 h | inhibits LPA-induced ovarian cancer cell motility | ||
| Jurkat | Growth Inhibition Assay | 50 μM | 24/48/72 h | enhances TRAIL-induces cell growth inhibition | ||
| SUPT1 | Growth Inhibition Assay | 50 μM | 24/48/72 h | enhances TRAIL-induces cell growth inhibition | ||
| Jurkat | Apoptosis Assay | 50 μM | 24/48 h | enhances TRAIL-induces cell apoptosis | ||
| SUPT1 | Apoptosis Assay | 50 μM | 24/48 h | enhances TRAIL-induces cell apoptosis | ||
| Cliquez pour voir plus de données expérimentales sur les lignées cellulaires | ||||||
Informations chimiques, stockage et stabilité
| Poids moléculaire | 294.30 | Formule | C17H14N2O3 |
Stockage (À partir de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 133550-30-8 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | Tyrphostin B42, Zinc02557947 | Smiles | C1=CC=C(C=C1)CNC(=O)C(=CC2=CC(=C(C=C2)O)O)C#N | ||
Solubilité
|
In vitro |
DMSO
: 58 mg/mL
(197.07 mM)
Ethanol : 9 mg/mL Water : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Entrez les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Entrez la formulation in vivo (Ceci nest que le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuiteμL PEG300, mélanger et clarifier, ajouter ensuiteμL Tween 80, mélanger et clarifier, ajouter ensuite μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuite μL Huile de maïs, mélanger et clarifier.
Remarque : 1. Assurez-vous que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue lors de lajout précédent est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
JAK2 (V617F)
EGFR
(Cell-free assay) 0.1 μM
|
|---|---|
| In vitro |
L'AG-490 inhibe la prolifération cellulaire dépendante de HER-2 avec un IC50 de 3,5 μM. Correspondant à l'inhibition spécifique dose-dépendante de JAK2 constitutivement activée dans les cellules de leucémie aiguë pré-B (ALL), ce composé (5 μM) bloque presque complètement la croissance de toutes les cellules ALL en induisant la mort cellulaire programmée, sans effet délétère sur l'hématopoïèse normale. Ce produit chimique n'inhibe pas les activités de Lck, Lyn, Btk, Syk et Src. Il (60-100 μM) bloque l'activation constitutive de Stat3sm et inhibe la croissance spontanée ainsi que celle induite par l'interleukine 2 des cellules tumorales de mycosis fongoïde (MF) avec des valeurs IC50 de 75 μM et 20 μM, respectivement. Ce composé inhibe puissamment la croissance des lymphocytes T humains médiée par l'IL-2 avec un IC50 de 25 μM en bloquant les activités de JAK3 et STAT5a/b. Il inhibe significativement l'activation constitutive de Stat3 dans les cellules MOPC, MPC11 et S194, entraînant une apoptose dramatique dose-dépendante. Ce produit chimique (100 μM) inhibe la phosphorylation d'Akt, inhibe l'activation du facteur nucléaire-κB et provoque l'activation de GSK-3β, entraînant la réduction de c-Myc. Il (50 μM) peut induire l'apoptose des cellules BaF3 exprimant les mutants T315I et E255K de Bcr-Abl. Ce composé à 30 μM inhibe non seulement la phosphorylation de JAK2 de type sauvage induite par l'Epo, mais aussi la phosphorylation constitutive du mutant JAK2 V617F. Il inhibe également puissamment la croissance cellulaire indépendante des cytokines induite par le mutant JAK2 V617F dans les cellules BaF3. |
| Kinase Assay |
Autophosphorylation de la kinase in vitro
|
|
L'AG-490 est dissous dans du DMSO 10%-H2O-éthanol 45%. Les extraits membranaires bruts (0,125 μg/mL) sont préactivés avec de l'EGF (20 nM) dans un tampon HEPES 50 mM, pH 7,6, et 125 mM NaCl, pendant 15 minutes à 4 °C. L'activité d'autophosphorylation de la kinase EGFR ou ErbB2 est dosée à 4 °C pendant 30 secondes dans des plaques de 96 puits en forme de V. Les extraits membranaires (8 μL) sont ajoutés à chaque puits contenant le mélange réactionnel (12 μL, 50 mM, HEPES, pH 7,4, 125 mM NaCl, 12 mM M8Ac2, 2 mM MnCl2, 1 mM NaVO3, 1 μM ATP, et 1 μCi[γ-32P]ATP, concentrations finales) et des concentrations croissantes de ce composé (4 μL). Après terminaison par addition de tampon d'échantillon chaud, les échantillons sont analysés sur un mini-gel d'électrophorèse sur gel de polyacrylamide-SDS à 6%, les gels sont séchés et une autoradiographie est effectuée pendant la période d'exposition linéaire. Les bandes du récepteur sont scannées densitrométriquement, et les résultats sont analysés par le programme Ez-Fit. Pour l'analyse de l'autophosphorylation de JAK2, JAK2 est immunoprécipité à l'aide d'un anticorps anti-JAK2 à partir de lysats de cellules G2 prétraitées pendant 16 heures avec des concentrations croissantes de ce produit chimique (0-50 μM). Les complexes immuns sont ensuite immunotransférés avec un anticorps anti-phosphotyrosine. Une inhibition dose-dépendante de l'activité kinase in vitro est démontrée en évaluant l'autophosphorylation de JAK2.
|
|
| In vivo |
L'administration d'AG-490 réduit drastiquement le nombre de cellules CD45+ et HLA-DR+ de 48% et 46% dans la moelle osseuse de souris non traitées, ainsi que de 38% et 22% dans la rate de souris non traitées à des niveaux indétectables. L'administration in vivo de ce composé provoque l'apoptose des cellules tumorales de myélome murin mais n'inhibe pas l'activation des macrophages médiée par l'IL-12 et la production d'IFN-γ par les lymphocytes. Conformément au blocage in vitro de l'activité du mutant JAK2 V617F, le traitement avec ce produit chimique à 0,5 mg/jour pendant 10 jours inhibe efficacement la tumorigenèse et l'invasion des cellules tumorales induites par le mutant JAK2 V617F chez les souris nues. La thérapie combinée avec cet agent et l'IL-12 induit des effets antitumoraux plus importants que l'un ou l'autre agent seul dans un modèle de tumeur de myélome murin. |
Références |
|
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
Questions fréquemment posées
Question 1:
I would like to know whether it (S1143) goes to CNS through BBB, or not?
Réponse :
It can go through the BBB, as shown in this reference: http://bloodjournal.hematologylibrary.org/content/111/4/2062.full.html.
