réservé à la recherche
Donafenib (Sorafenib D3) Raf inhibiteur
N° Cat.S9621
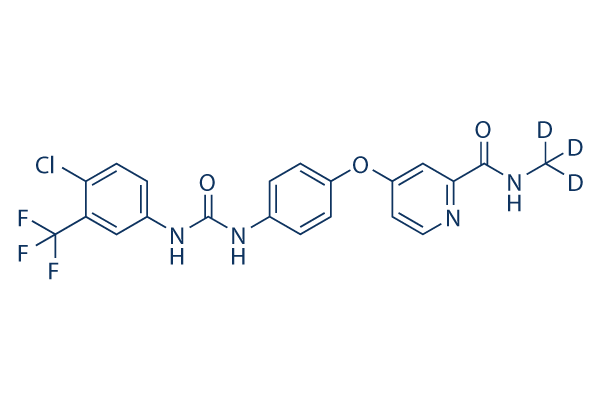
Structure chimique
Poids moléculaire: 467.84
Contrôle qualité
- Cité dans Nature Medicine pour sa qualité supérieure
- COA
- NMR
- HPLC
- SDS
- Fiche technique
| Cibles apparentées | ERK p38 MAPK JNK MEK Ras KRas S6 Kinase MAP4K TAK1 Mixed Lineage Kinase |
|---|---|
| Autre Raf Inhibiteurs | LY3009120 Exarafenib (KIN-2787) GDC-0879 Avutometinib (Ro5126766, CH5126766) PLX-4720 AZ 628 SB590885 TAK-632 GW5074 RAF265 (CHIR-265) |
Informations chimiques, stockage et stabilité
| Poids moléculaire | 467.84 | Formule | C21H13D3ClF3N4O3 |
Stockage (À partir de la date de réception) | 3 years -20°C powder |
|---|---|---|---|---|---|
| N° CAS | 1130115-44-4 | -- | Stockage des solutions mères |
|
|
| Synonymes | Bay 43-9006 D3, CM-4307 | Smiles | CNC(=O)C1=NC=CC(=C1)OC2=CC=C(C=C2)NC(=O)NC3=CC(=C(C=C3)Cl)C(F)(F)F | ||
Solubilité
|
In vitro |
DMSO
: 94 mg/mL
(200.92 mM)
Ethanol : 6 mg/mL Water : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Entrez les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Entrez la formulation in vivo (Ceci nest que le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuiteμL PEG300, mélanger et clarifier, ajouter ensuiteμL Tween 80, mélanger et clarifier, ajouter ensuite μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuite μL Huile de maïs, mélanger et clarifier.
Remarque : 1. Assurez-vous que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue lors de lajout précédent est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
Raf-1
(Cell-free assay) 6 nM
mVEGFR-2
(Cell-free assay) 15 nM
mVEGFR-3
(Cell-free assay) 20 nM
B-Raf
(Cell-free assay) 22 nM
|
|---|---|
| In vitro |
BAY 43-9006 supprime l'activité de BRAF de type sauvage et de la forme mutante V599E in vitro. De plus, BAY 43-9006 démontre une activité significative contre plusieurs récepteurs tyrosine kinases impliqués dans la néovascularisation et la progression tumorale, y compris le récepteur du facteur de croissance endothélial vasculaire (VEGFR)-2, VEGFR-3, le récepteur du facteur de croissance dérivé des plaquettes β, Flt-3 et c-KIT. Dans les essais mécanistiques cellulaires, BAY 43-9006 démontre une inhibition de la voie de la mitogen-activated protein kinase dans les lignées cellulaires de tumeurs du côlon, du pancréas et du sein exprimant KRAS mutant ou BRAF de type sauvage ou mutant, tandis que les lignées cellulaires de cancer du poumon non à petites cellules exprimant KRAS mutant sont insensibles à l'inhibition de la voie de la mitogen-activated protein kinase par BAY 43-9006. Une puissante inhibition de l'autophosphorylation des récepteurs cellulaires VEGFR-2, du récepteur du facteur de croissance dérivé des plaquettes β et de VEGFR-3 est également observée pour BAY 43-9006. |
| In vivo |
L'administration orale quotidienne de BAY 43-9006 démontre une activité antitumorale à large spectre dans des modèles de xénogreffes de cancer du côlon, du sein et du poumon non à petites cellules. L'immunohistochimie démontre une association étroite entre l'inhibition de la croissance tumorale et l'inhibition de la phosphorylation des kinases régulées par le signal extracellulaire (ERKs) 1/2 dans deux des trois modèles de xénogreffes examinés, ce qui est cohérent avec l'inhibition de la voie RAF/MEK/ERK dans certains modèles mais pas tous. Des analyses supplémentaires de la densité des microvaisseaux et de la surface des microvaisseaux dans les mêmes sections tumorales utilisant des anticorps anti-souris CD31 démontrent une inhibition significative de la néovascularisation dans les trois modèles de xénogreffes. |
Références |
|
Informations sur lessai clinique
(données de https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Sponsor/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT04612712 | Recruiting | Advanced Gastrointestinal Tumors |
Suzhou Zelgen Biopharmaceuticals Co.Ltd|Jiangsu Alphamab Biopharmaceuticals Co. Ltd |
January 19 2021 | Phase 1|Phase 2 |
| NCT04816123 | Completed | Healthy Male Adult |
Suzhou Zelgen Biopharmaceuticals Co.Ltd |
October 9 2018 | Phase 1 |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
