réservé à la recherche
Aliskiren Hemifumarate RAAS inhibiteur
N° Cat.S2199
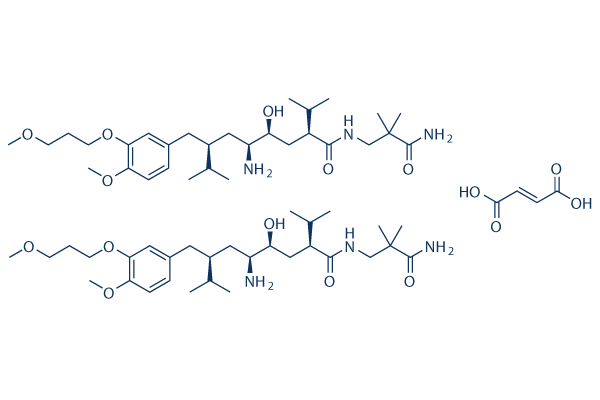
Structure chimique
Poids moléculaire: 609.83
Contrôle qualité
| Cibles apparentées | Adrenergic Receptor Estrogen/progestogen Receptor GPR Androgen Receptor Glucocorticoid Receptor ACE Progesterone Receptor Opioid Receptor PGES THR |
|---|---|
| Autre RAAS Inhibiteurs | Temocapril HCl Imidapril HCl VTP-27999 TFA Temocapril Zofenopril calcium Delapril Hydrochloride |
Informations chimiques, stockage et stabilité
| Poids moléculaire | 609.83 | Formule | C30H53N3O6.1/2C4H4O4 |
Stockage (À partir de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 173334-58-2 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | CGP 60536 hemifumarate, CGP60536B hemifumarate, SPP 100 hemifumarate | Smiles | CC(C)C(CC1=CC(=C(C=C1)OC)OCCCOC)CC(C(CC(C(C)C)C(=O)NCC(C)(C)C(=O)N)O)N.CC(C)C(CC1=CC(=C(C=C1)OC)OCCCOC)CC(C(CC(C(C)C)C(=O)NCC(C)(C)C(=O)N)O)N.C(=CC(=O)O)C(=O)O | ||
Solubilité
|
In vitro |
DMSO
: 122 mg/mL
(200.05 mM)
Water : 122 mg/mL Ethanol : 122 mg/mL |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Entrez les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Entrez la formulation in vivo (Ceci nest que le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuiteμL PEG300, mélanger et clarifier, ajouter ensuiteμL Tween 80, mélanger et clarifier, ajouter ensuite μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuite μL Huile de maïs, mélanger et clarifier.
Remarque : 1. Assurez-vous que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue lors de lajout précédent est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
Renin
1.5 nM
|
|---|---|
| In vitro |
Aliskiren Hemifumarate semble se lier à la fois à la poche de liaison hydrophobe S1/S3 et à une grande sous-poche distincte qui s'étend du site de liaison S3 vers le cœur hydrophobe de la rénine. La biodisponibilité orale de l'Aliskiren Hemifumarate est de 2,4 % chez les rats, 16 % chez les ouistitis et environ 2,5 % chez l'homme. |
| In vivo |
Aliskiren Hemifumarate (< 10 mg/kg, oral) inhibe l'activité rénine plasmatique et abaisse la pression artérielle chez les ouistitis privés de sodium. Un traitement oral quotidien par Aliskiren Hemifumarate abaisse efficacement la pression artérielle, avec un profil de sécurité et de tolérance favorable, chez les patients souffrant d'hypertension légère à modérée. |
Références |
|
Informations sur lessai clinique
(données de https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Sponsor/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT04432350 | Withdrawn | COVID|Drug Effect|Drug Interaction|Risk Reduction |
Tabula Rasa HealthCare |
June 12 2020 | -- |
| NCT01570686 | Completed | Hypertension |
Novartis Pharmaceuticals|Novartis |
April 2012 | Phase 4 |
| NCT01519635 | Completed | Hypertension |
Centre Hospitalier Universitaire Vaudois |
October 2011 | Phase 4 |
| NCT01235910 | Terminated | Hypertension|Cardiac Transplantation |
University of Colorado Denver|American Heart Association |
May 2011 | Phase 4 |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
