réservé à la recherche
Orteronel P450 (e.g. CYP17) inhibiteur
N° Cat.S1195
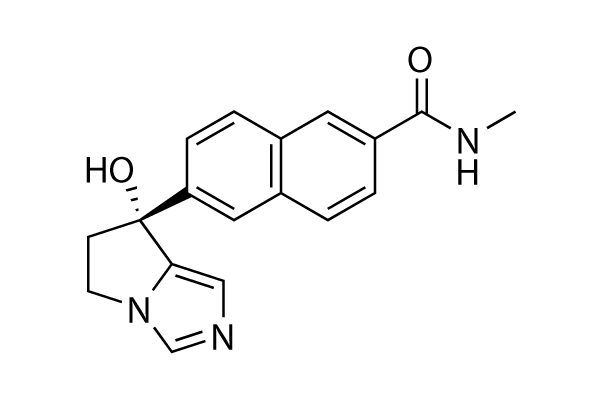
Structure chimique
Poids moléculaire: 307.35
Contrôle qualité
| Cibles apparentées | Dehydrogenase HSP Transferase PDE phosphatase PPAR Vitamin Carbohydrate Metabolism Mitochondrial Metabolism Drug Metabolite |
|---|---|
| Autre P450 (e.g. CYP17) Inhibiteurs | Apigenin Baicalein Avasimibe Naringenin Diosmetin Alizarin Benzbromarone Sodium Danshensu Naringin Piperine |
Informations chimiques, stockage et stabilité
| Poids moléculaire | 307.35 | Formule | C18H17N3O2 |
Stockage (À partir de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 426219-18-3 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | TAK-700 | Smiles | CNC(=O)C1=CC2=C(C=C1)C=C(C=C2)C3(CCN4C3=CN=C4)O | ||
Solubilité
|
In vitro |
DMSO
: 61 mg/mL
(198.47 mM)
Ethanol : 8 mg/mL Water : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Entrez les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Entrez la formulation in vivo (Ceci nest que le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuiteμL PEG300, mélanger et clarifier, ajouter ensuiteμL Tween 80, mélanger et clarifier, ajouter ensuite μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuite μL Huile de maïs, mélanger et clarifier.
Remarque : 1. Assurez-vous que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue lors de lajout précédent est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
17,20-lyase (Human)
38 nM
17,20-lyase (Rat)
54 nM
|
|---|---|
| In vitro |
In vitro, le TAK-700 montre une activité inhibitrice puissante contre la stéroïde 17,20-lyase de rat et humaine avec une IC50 de 54 nM et 38 nM, respectivement. Tandis que d'autres isoformes du CYP, y compris la 11-hydroxylase et le CYP3A4, ne sont pas significativement affectées par ce composé. Dans les microsomes exprimant les isoformes du CYP humain, cette substance chimique présente des effets inhibiteurs plus importants sur la 17,20-lyase avec une IC50 de 19 nM par rapport aux autres isoformes du CYP. Ce composé montre une activité inhibitrice contre la 17,20-lyase et la 17-hydroxylase de singe avec une IC50 de 27 nM et 38 nM, respectivement. Dans les cellules surrénales de singe, cette substance chimique inhibe la production stimulée par l'ACTH de DHEA et d'androstenedione avec une IC50 de 110 nM et 130 nM, respectivement. De plus, ce composé inhibe également puissamment la production de DHEA dans les cellules de la lignée tumorale corticosurrénalienne humaine H295R avec une IC50 de 37 nM. |
| In vivo |
Chez les singes cynomolgus, un traitement oral d'Orteronel (TAK-700) à une dose de 1 mg/kg réduit notablement les niveaux sériques de testostérone et de déhydroépiandrostérone (DHEA). Le traitement oral de ce composé à une dose de 1 mg/kg entraîne des paramètres pharmacocinétiques favorables avec une Tmax, Cmax, t1/2 et AUC0-24 heures de 1,7 heures, 0,147 μg/mL, 3,8 heures et 0,727 μg h/mL, respectivement. |
Références |
|
Informations sur lessai clinique
(données de https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Sponsor/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT01808040 | Completed | Post Menopausal Hormone Receptor Positive Breast Cancer |
University of Wisconsin Madison|Millennium Pharmaceuticals Inc. |
November 2012 | Phase 1 |
| NCT01666314 | Completed | Prostate Cancer |
Millennium Pharmaceuticals Inc.|Takeda |
August 20 2012 | Phase 1|Phase 2 |
| NCT01549951 | Completed | Prostate Cancer |
Millennium Pharmaceuticals Inc. |
May 2012 | Phase 2 |
| NCT01084655 | Completed | Prostate Cancer |
Millennium Pharmaceuticals Inc.|Takeda |
July 2010 | Phase 1|Phase 2 |
| NCT01046916 | Completed | Prostate Cancer |
Millennium Pharmaceuticals Inc. |
May 2010 | Phase 2 |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
