réservé à la recherche
Ribavirin (ICN-1229) Antiviral chimique
N° Cat.S2504
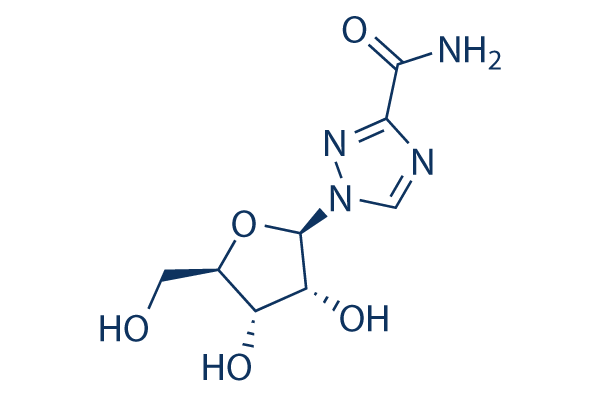
Structure chimique
Poids moléculaire: 244.20864
Contrôle qualité
| Cibles apparentées | Integrase Bacterial Antibiotics Anti-infection Fungal COVID-19 Parasite Reverse Transcriptase HIV HCV Protease |
|---|---|
| Autre Antiviral Inhibiteurs | Moroxydine HCl Aloperine GS-441524 Oleanolic Acid Harringtonine NGI-1 U18666A Aloin B Saikosaponin B2 Lapachol |
Culture cellulaire, traitement et concentration de travail
| Lignées cellulaires | Type dessai | Concentration | Temps dincubation | Formulation | Description de lactivité | PMID |
|---|---|---|---|---|---|---|
| E6SM cell lines | Function assay | Effective concentration required to inhibit Herpes simplex virus-1(HSV-1) / thymine kinase deficient (TK-)B2006 / VMW1837 induced cytopathicity by 50% in E6SM cell lines, EC50=0.005 μM | ||||
| MDCK cells | Function assay | 3 days | Antiviral activity against Influenza B virus (B/HK/5/72) infected in MDCK cells assessed as virus-induced cytopathic effect after 3 days by microscopic analysis, EC50=0.094 μM | |||
| mouse L1210 cells | Function assay | 20-60 mins | Inhibition of IMPDH in mouse L1210 cells assessed as formation of [2,8-3H]hypoxanthine from [2,8-3H]IMP after 20 to 60 mins, IC50=1 μM | |||
| human CEM cells | Function assay | 20-60 mins | Inhibition of IMPDH in human CEM cells assessed as formation of [2,8-3H]hypoxanthine from [2,8-3H]IMP after 20 to 60 mins, IC50=1 μM | |||
| BHK21 cell line | Function assay | Inhibition of West Nile virus VLP replicon in BHK21 cell line, EC50=1.1 μM | ||||
| HeLa cell | Function assay | Effective concentration required to inhibit respiratory synaptial(RSV) virus-induced cytopathicity by 50% in HeLa cell lines, EC50=1.5 μM | ||||
| MDCK cells | Function assay | 36 h | Antiinfluenza activity against influenza A virus H1N1 infected in MDCK cells assessed as inhibition of virus-induced cytopathic effect after 36 hrs, IC50=1.9 μM | |||
| MDBK cells | Function assay | 2 days | Antiviral activity against Bovine viral diarrhea virus 1-NADL ATCC VR534 infected in MDBK cells assessed as reduction of viral cytopathic effect after 2 days bt MTS assay, EC50=4.6 μM | |||
| african green monkey Vero cells | Function assay | 5 days | Antiviral activity against RSV A2 infected in african green monkey Vero cells after 5 days by plaque reduction assay, EC50=7 μM | |||
| HEL cells | Function assay | 2-3 days | Antiviral activity against Herpes simplex virus 1 KOS infected in HEL cells assessed as protection from virus-induced cytopathogenicity after 2 to 3 days by MTT assay, EC50=10 μM | |||
| HEK293 cells | Function assay | 24 h | Inhibition of influenza A virus RNA-dependent RNA polymerase expressed in HEK293 cells after 24 hrs by dual luciferase reporter gene assay, EC50=15 μM | |||
| human BE(2)-C cells | Function assay | 18-20 h | Antiviral activity against Western equine encephalomyelitis virus infected in human BE(2)-C cells assessed as inhibition of viral RNA replication after 18 to 20 hrs by luciferase reporter gene assay, IC50=16 μM | |||
| human HuH7-J20 cells | Function assay | Antiviral activity against HCV JFH1 infected in human HuH7-J20 cells assessed as inhibition of viral life cycle by measuring secreted alkaline phosphatase level preincubated with cells for 1 hr followed by viral inoculation for 3 hrs measured at 72 hrs, EC50=30.4 μM | ||||
| human MT4 cells | Cytotoxic assay | 96 h | Cytotoxicity against human MT4 cells after 96 hrs by MTT assay, CC50=31 μM | |||
| human HuH7 cells | Cytotoxic assay | 3 days | Cytotoxicity against human HuH7 cells infected with HCV1b after 3 days by MTS assay, CC50=32 μM | |||
| human KB cells | Function assay | 72 h | Antiviral activity against Rhinovirus type 13 infected in human KB cells assessed as inhibition of virus-induced cytopathic effect after 72 hrs relative to control | |||
| human KB cells | Function assay | 1-1000 μg/ml | 72 h | Antiviral activity against Rhinovirus type 13 infected in human KB cells assessed as inhibition of virus-induced cytopathic effect at 1 to 1000 ug/ml after 72 hrs | ||
| Cliquez pour voir plus de données expérimentales sur les lignées cellulaires | ||||||
Informations chimiques, stockage et stabilité
| Poids moléculaire | 244.20864 | Formule | C8H12N4O5 |
Stockage (À partir de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 36791-04-5 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | NSC-163039, RTCA, Tribavirin | Smiles | C1=NC(=NN1C2C(C(C(O2)CO)O)O)C(=O)N | ||
Solubilité
|
In vitro |
DMSO
: 49 mg/mL
(200.64 mM)
Water : 49 mg/mL Ethanol : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Entrez les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Entrez la formulation in vivo (Ceci nest que le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuiteμL PEG300, mélanger et clarifier, ajouter ensuiteμL Tween 80, mélanger et clarifier, ajouter ensuite μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuite μL Huile de maïs, mélanger et clarifier.
Remarque : 1. Assurez-vous que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue lors de lajout précédent est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| In vitro |
Ribavirin (ICN-1229) réduit significativement l'efficacité avec laquelle les réplicons subgénomiques descendants transfectent de nouvelles cellules dans le système réplicon, bien qu'il ait peu d'effet sur les niveaux de réplication du VHC. Ce composé augmente la fréquence de mutation du VHC, les taux les plus élevés de mutations étant trouvés dans la région codant pour NS5A. Il améliore la production de TH1 tout en inhibant la production de cytokines T2 par les lymphocytes T stimulés. Ribavirin montre une activité antivirale contre une variété de virus à ARN et est utilisé en combinaison avec l'interféron-alpha pour traiter l'infection par le virus de l'hépatite C. Il réduit la production de poliovirus infectieux à seulement 0,00001% en culture cellulaire. Son activité antivirale est exercée directement par une mutagenèse létale du matériel génétique viral. Ce composé réduit nettement les paramètres d'activation des macrophages induits par le virus à des concentrations physiologiques (jusqu'à 500 mg/mL). Il inhibe la production d'IL-4 par les cellules Th2, tandis qu'il ne diminue pas la production d'IFN-gamma dans les cellules Th1. Ribavirin présente une activité antivirale contre un large éventail de virus à ADN et à ARN in vitro. C'est un agent cytostatique et provoque une réduction de la synthèse de l'ADN, de l'ARN et des protéines dans les cellules exposées. On pense qu'il induit un changement de phénotype des lymphocytes T-helper de type 2 à type 1.
|
Références |
|
|---|
Applications
| Méthodes | Biomarqueurs | Images | PMID |
|---|---|---|---|
| Western blot | p53 / p-p53 / p21 / Mdm2 EZH2 / p-ERK / ERK / p-eIF4E / eIF4E / p21 Cyclin D1 p-AKT / AKT / pBP1 / BP1 |

|
22962590 |
| Growth inhibition assay | Cell number |
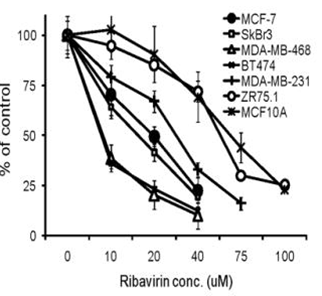
|
21415224 |
Informations sur lessai clinique
(données de https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Sponsor/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT05940545 | Recruiting | CCHF |
Liverpool School of Tropical Medicine |
July 12 2023 | Phase 1|Phase 2 |
| NCT04283513 | Not yet recruiting | Hemorrhagic Fever |
U.S. Army Medical Research and Development Command |
October 31 2022 | Phase 2 |
| NCT04335123 | Completed | COVID-19 |
University of Kansas Medical Center |
April 4 2020 | Phase 1 |
| NCT04285034 | Completed | Lassa Fever |
University of Oxford |
November 26 2019 | -- |
| NCT03889106 | Terminated | Lassa Fever |
University of Oxford|National Institute for Health Research United Kingdom|Kenema Government Hospital|London School of Hygiene and Tropical Medicine|Public Health England |
March 1 2019 | -- |
| NCT03585725 | Terminated | Follicular Lymphoma|Mantle Cell Lymphoma |
Weill Medical College of Cornell University|Memorial Sloan Kettering Cancer Center |
September 26 2018 | Early Phase 1 |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
