Données techniques
| Formule | C13H13N3OS |
||||||
| Poids moléculaire | 259.33 | N° CAS | 4311-88-0 | ||||
| Solubilité (25°C)* | In vitro | DMSO | 52 mg/mL (200.51 mM) | ||||
| Water | Insoluble | ||||||
| Ethanol | Insoluble | ||||||
| In Vivo (Ajoutez les solvants au produit individuellement et dans lordre.) |
|
||||||
|
* <1 mg/ml signifie légèrement soluble ou insoluble. * Veuillez noter que Selleck teste la solubilité de tous les composés en interne, et la solubilité réelle peut différer légèrement des valeurs publiées. Ceci est normal et est dû à de légères variations dun lot à lautre. * Expédition à température ambiante (les tests de stabilité montrent que ce produit peut être expédié sans aucune mesure de refroidissement.) |
|||||||
Préparation des solutions mères
Activité biologique
| Description | Necrostatin-1 (Nec-1) est un inhibiteur spécifique de RIP1 (RIPK1) et inhibe la nécroptose induite par le TNF-α avec une EC50 de 490 nM dans les cellules 293T. Necrostatin-1 bloque également IDO et supprime l'autophagy et l'apoptosis. | ||||
|---|---|---|---|---|---|
| Cibles |
|
||||
| In vitro | La Necrostatin-1 (1-100 μM) inhibe l'autophosphorylation de RIP1 surexprimée et endogène. Il est constaté que RIP1 est la cible cellulaire primaire responsable de l'activité antinécroptose de ce composé. Ce produit chimique supprime efficacement la mort cellulaire nécroptotique déclenchée par une série de stimuli dans une variété de types cellulaires. Il, précédemment identifié comme un inhibiteur de petite molécule de nécroptose, inhibe la nécroptose induite par RIP kinase et inhibe la nécroptose induite par TNF-α dans les cellules Jurkat avec une EC50 de 490 nM. |
||||
| In Vivo | La Necrostatin-1 (Nec-1) est un inhibiteur spécifique de petite molécule de la protéine kinase 1 interagissant avec le récepteur (RIPK1) qui inhibe spécifiquement la phosphorylation de ce composé. |
||||
| Caractéristiques | Un outil puissant pour caractériser le rôle de la nécroptose avec une cible primaire caractérisée. |
Protocole (de référence)
| Test kinase : |
|
|---|---|
| Test cellulaire : |
|
| Étude animale : |
|
Références
|
Validation du produit par le client
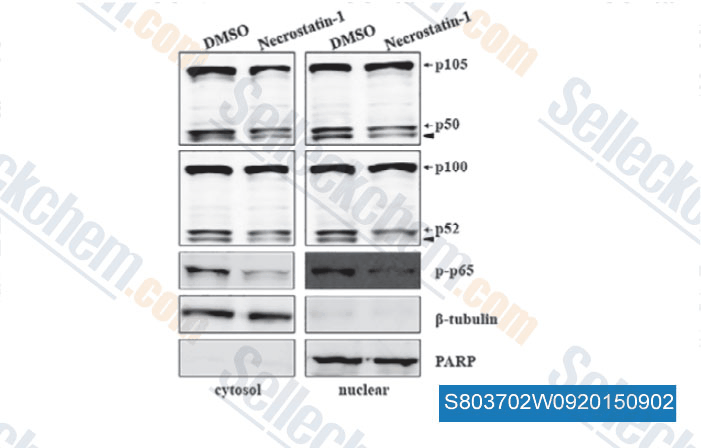
-
Données de [ , , J Cell Mol Med, 2015, 19(5): 1042-54 ]
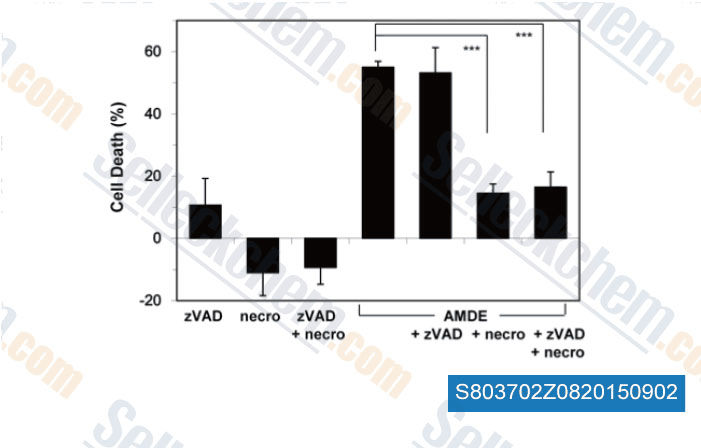
-
Données de [ , , PLoS One, 2015, 10(3): e0122083 ]
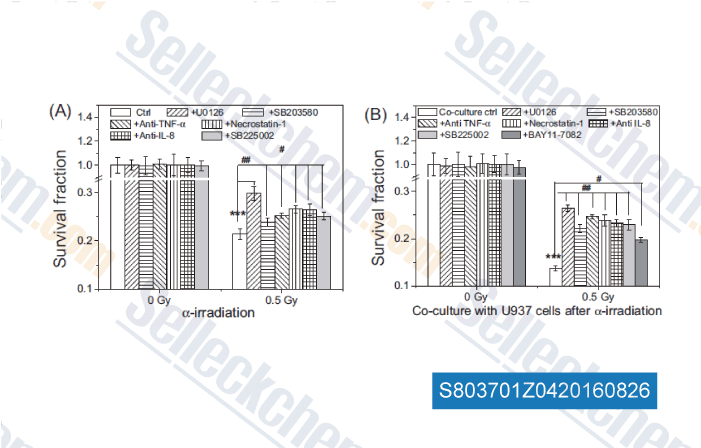
-
Données de [ , , Mutation Research, 2016, 789:1-8. ]
De Selleck Necrostatin-1 (Nec-1) A été cité par 321 Publications
| Soluble tissue factor generated by necroptosis-triggered shedding is responsible for thrombosis [ Cell Res, 2025, 10.1038/s41422-025-01167-8] | PubMed: 40940518 |
| The noncanonical function of liver-type phosphofructokinase potentiates the efficacy of HDAC inhibitors in cancer [ Signal Transduct Target Ther, 2025, 10(1):341] | PubMed: 41083431 |
| LINE-1 ORF1p Mimics Viral Innate Immune Evasion Mechanisms in Pancreatic Ductal Adenocarcinoma [ Cancer Discov, 2025, 10.1158/2159-8290.CD-24-1317] | PubMed: 39919290 |
| Ferroptosis-activating metabolite acrolein antagonizes necroptosis and anti-cancer therapeutics [ Nat Commun, 2025, 16(1):4919] | PubMed: 40425585 |
| Harnessing the FGFR2/NF2/YAP signaling-dependent necroptosis to develop an FGFR2/IL-8 dual blockade therapeutic strategy [ Nat Commun, 2025, 16(1):4128] | PubMed: 40319089 |
| Targeting pancreatic cancer glutamine dependency confers vulnerability to GPX4-dependent ferroptosis [ Cell Rep Med, 2025, 6(2):101928] | PubMed: 39879992 |
| GCLC desuccinylation regulated by oxidative stress protects human cancer cells from ferroptosis [ Cell Death Differ, 2025, 32(9):1679-1690] | PubMed: 40188196 |
| Carbon ion combined photon radiotherapy induces ferroptosis via NCOA4-mediated ferritinophagy in glioblastoma [ Redox Biol, 2025, 86:103865] | PubMed: 40925125 |
| SLC25A1 and ACLY maintain cytosolic acetyl-CoA and regulate ferroptosis susceptibility via FSP1 acetylation [ EMBO J, 2025, 10.1038/s44318-025-00369-5] | PubMed: 39881208 |
| Akt isoform specificity drives intrinsic immune regulation during HSV-1 infection [ Proc Natl Acad Sci U S A, 2025, 122(27):e2504962122] | PubMed: 40601626 |
POLITIQUE DE RETOUR
La politique de retour inconditionnelle de Selleck Chemical garantit une expérience dachat en ligne fluide à nos clients. Si vous nêtes en aucun cas satisfait de votre achat, vous pouvez retourner tout article dans les 7 jours suivant sa réception. En cas de problèmes de qualité du produit, quil sagisse de problèmes liés au protocole ou au produit, vous pouvez retourner tout article dans les 365 jours suivant la date dachat initiale. Veuillez suivre les instructions ci-dessous lors du retour des produits.
EXPÉDITION ET STOCKAGE
Les produits Selleck sont transportés à température ambiante. Si vous recevez le produit à température ambiante, soyez assuré que le service dinspection de la qualité de Selleck a mené des expériences pour vérifier que le placement à température normale pendant un mois naffectera pas lactivité biologique des produits en poudre. Après réception, veuillez stocker le produit conformément aux exigences décrites dans la fiche technique. La plupart des produits Selleck sont stables dans les conditions recommandées.
NON DESTINÉ À UN USAGE HUMAIN, VÉTÉRINAIRE DIAGNOSTIQUE OU THÉRAPEUTIQUE.
