Données techniques
| Formule | C26H19F3N4O |
||||||
| Poids moléculaire | 460.45 | N° CAS | 742112-33-0 | ||||
| Solubilité (25°C)* | In vitro | DMSO | 92 mg/mL (199.8 mM) | ||||
| Ethanol | 8 mg/mL (17.37 mM) | ||||||
| Water | Insoluble | ||||||
| In Vivo (Ajoutez les solvants au produit individuellement et dans lordre.) |
|
||||||
|
* <1 mg/ml signifie légèrement soluble ou insoluble. * Veuillez noter que Selleck teste la solubilité de tous les composés en interne, et la solubilité réelle peut différer légèrement des valeurs publiées. Ceci est normal et est dû à de légères variations dun lot à lautre. * Expédition à température ambiante (les tests de stabilité montrent que ce produit peut être expédié sans aucune mesure de refroidissement.) |
|||||||
Préparation des solutions mères
Activité biologique
| Description | OSU-03012 (AR-12) est un puissant inhibiteur de la PDK-1(phosphoinositide-dependent kinase 1) recombinante avec une IC50 de 5 μM dans un essai acellulaire, montrant une augmentation de 2 fois de la puissance par rapport à OSU-02067. | ||
|---|---|---|---|
| Cibles |
|
||
| In vitro | OSU-03012 (AR-12) induit la mort apoptotique dans les cellules PC-3 avec une IC50 de 5 µM et réduit l'activité de la p70S6K immunoprécipitée. Il supprime complètement la croissance cellulaire dans une gamme diversifiée de lignées de cellules tumorales à des concentrations de 3–5 μm, par rapport à la concentration d'au moins 50 μm. Ce composé favorise la mort cellulaire à un degré plus élevé dans les cellules de gliome que dans les astrocytes non transformés. Il provoque une induction dose-dépendante de la mort cellulaire qui n'est pas altérée par la mutation p53, l'expression de l'ERBB1 VIII ou la perte de fonction de la phosphatase et de la tensine due à une délétion homologue sur le chromosome 10. OSU-03012 et les rayonnements ionisants provoquent une élévation additive, indépendante des caspases, de la mort cellulaire. Sa létalité en tant qu'agent unique ou lorsqu'il est combiné avec des modulateurs de signalisation n'est pas modifiée dans les cellules dépourvues d'expression de BIM ou de BAX/BAK. Il favorise la libération de la cathepsine B du compartiment lysosomal et celle de l'AIF des mitochondries. La létalité de ce composé est atténuée dans les cellules protéine kinase R-like endoplasmic reticulum kinase-/- , ce qui est corrélé à la réduction du clivage de BID et à la suppression de la libération de cathepsine B et d'AIF dans le cytosol. Il inhibe la prolifération et la migration des cellules cancéreuses thyroïdiennes (cellules NPA, WRO et ARO) et induit l'apoptose, ce qui entraîne une augmentation des cellules en phase S sans augmentation des cellules en G2. OSU-03012 est un inhibiteur ATP-compétitif de l'activité de PAK et supprime la phosphorylation d'AKT dans les cellules cancéreuses thyroïdiennes. Il inhibe la croissance cellulaire des lignées de cellules de carcinome hépatocellulaire, y compris les cellules Huh7, Hep3B et HepG2 avec des valeurs d'IC50 inférieures à 1 μM. Ce composé ne supprime pas l'activité de PDK1 ou d'AKT ou n'induit pas l'apoptose cellulaire, mais induit l'autophagie dans les cellules Huh7. De plus, une accumulation d'espèces réactives de l'oxygène (ROS) est détectée après son traitement. Une étude récente montre qu'il pourrait améliorer la susceptibilité des lignées cellulaires mutantes (Bcr)-Abl à l'apoptose induite. |
||
| In Vivo | OSU-03012 (AR-12) supprime la croissance tumorale de 57,59% et augmente la LC3 clivée dans les xénogreffes tumorales Huh7 à 200 mg/kg. Ce composé diminue remarquablement l'expression de la protéine EGFR dans les tumeurs de 48% par rapport aux contrôles du véhicule et empêche également YB-1 de se lier au promoteur de l'EGFR dans les xénogreffes MDA-MB-435/LCC6. Il est bien toléré et inhibe la croissance des xénogreffes de schwannome HMS-97 de 55% après administration orale. |
Protocole (de référence)
| Test kinase : |
|
|---|---|
| Test cellulaire : |
|
| Étude animale : |
|
Références
|
Validation du produit par le client
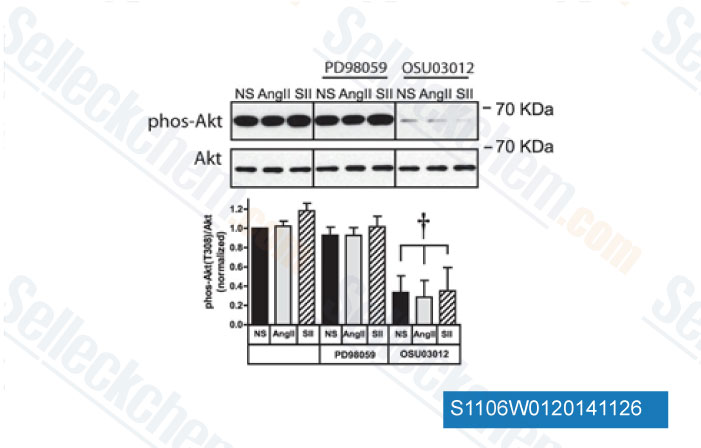
-
Données de [ J Biol Chem , 2014 , 289(38), 26155-66 ]
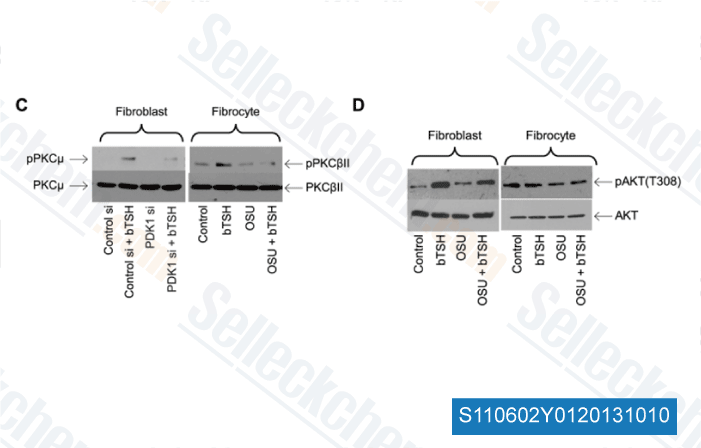
-
Données de [ PLoS One , 2013 , 8, e75100 ]
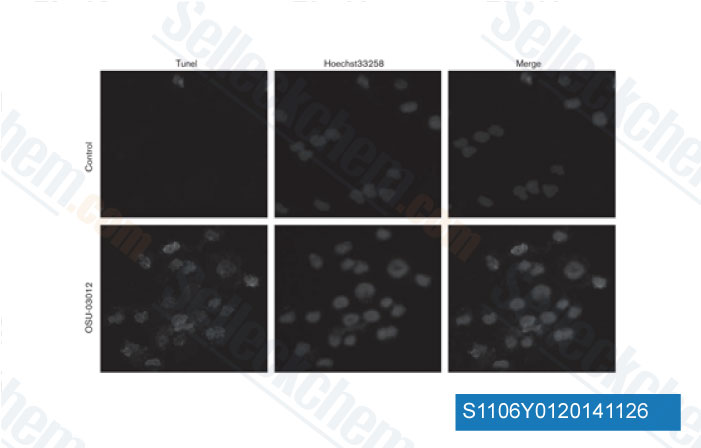
-
Données de [ Anticancer Drugs , 2013 , 24(7), 690-8 ]
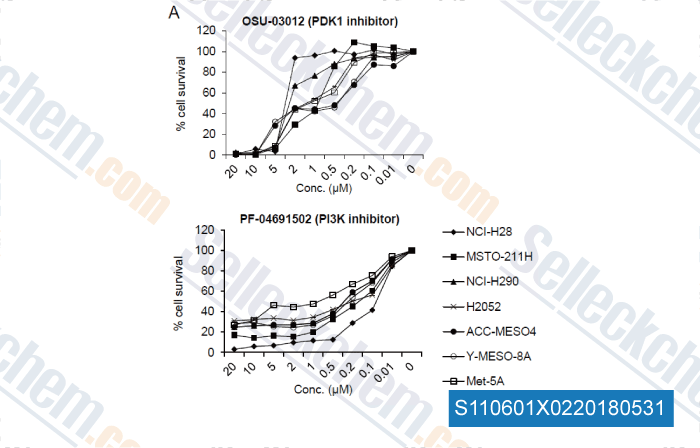
-
Données de [ , , Cancer Medicine, 2017, 6(11):2646-2659 ]
De Selleck OSU-03012 (AR-12) A été cité par 51 Publications
| R406 and its structural analogs reduce SNCA/α-synuclein levels via autophagic degradation [ Autophagy, 2025, 1-17.] | PubMed: 40143425 |
| NAC1 confines virus-specific memory formation of CD4+ T cells through the ROCK1-mediated pathway [ J Med Virol, 2023, 95(7):e28957] | PubMed: 37465969 |
| Salmonella effector SopF regulates PANoptosis of intestinal epithelial cells to aggravate systemic infection [ Gut Microbes, 2023, 15(1):2180315] | PubMed: 36803521 |
| AR12 increases BAG3 expression which is essential for Tau and APP degradation via LC3-associated phagocytosis and macroautophagy [ Aging (Albany NY), 2022, 14(20):8221-8242] | PubMed: 36227739 |
| Pulmonary fibrosis distal airway epithelia are dynamically and structurally dysfunctional [ Nat Commun, 2021, 12(1):4566] | PubMed: 34315881 |
| Development of potent dual PDK1/AurA kinase inhibitors for cancer therapy: Lead-optimization, structural insights, and ADME-Tox profile [ Eur J Med Chem, 2021, 226:113895] | PubMed: 34624821 |
| Decanoic Acid Stimulates Autophagy in D. discoideum [ Cells, 2021, 10(11)2946] | PubMed: 34831171 |
| Inhibition of heat shock proteins increases autophagosome formation, and reduces the expression of APP, Tau, SOD1 G93A and TDP-43 [ Aging (Albany NY), 2021, 13(13):17097-17117] | PubMed: 34252884 |
| OSU-03012 Disrupts Akt Signaling and Prevents Endometrial Carcinoma Progression in vitro and in vivo [ Drug Des Devel Ther, 2021, 15:1797-1810] | PubMed: 33958857 |
| Metabolic Modifier Screen Reveals Secondary Targets of Protein Kinase Inhibitors Within Nucleotide Metabolism [ Cell Chem Biol, 2020, 20;27(2):197-205.e6] | PubMed: 31734178 |
POLITIQUE DE RETOUR
La politique de retour inconditionnelle de Selleck Chemical garantit une expérience dachat en ligne fluide à nos clients. Si vous nêtes en aucun cas satisfait de votre achat, vous pouvez retourner tout article dans les 7 jours suivant sa réception. En cas de problèmes de qualité du produit, quil sagisse de problèmes liés au protocole ou au produit, vous pouvez retourner tout article dans les 365 jours suivant la date dachat initiale. Veuillez suivre les instructions ci-dessous lors du retour des produits.
EXPÉDITION ET STOCKAGE
Les produits Selleck sont transportés à température ambiante. Si vous recevez le produit à température ambiante, soyez assuré que le service dinspection de la qualité de Selleck a mené des expériences pour vérifier que le placement à température normale pendant un mois naffectera pas lactivité biologique des produits en poudre. Après réception, veuillez stocker le produit conformément aux exigences décrites dans la fiche technique. La plupart des produits Selleck sont stables dans les conditions recommandées.
NON DESTINÉ À UN USAGE HUMAIN, VÉTÉRINAIRE DIAGNOSTIQUE OU THÉRAPEUTIQUE.
