Données techniques
| Formule | C6H7N5 |
||||||||||
| Poids moléculaire | 149.15 | N° CAS | 5142-23-4 | ||||||||
| Solubilité (25°C)* | In vitro | DMSO (chauffé au bain-marie à 50 °C) | 10 mg/mL (67.04 mM) | ||||||||
| Ethanol | 10 mg/mL (67.04 mM) | ||||||||||
| Water | 4 mg/mL (26.81 mM) | ||||||||||
| In Vivo (Ajoutez les solvants au produit individuellement et dans lordre.) |
|
||||||||||
|
* <1 mg/ml signifie légèrement soluble ou insoluble. * Veuillez noter que Selleck teste la solubilité de tous les composés en interne, et la solubilité réelle peut différer légèrement des valeurs publiées. Ceci est normal et est dû à de légères variations dun lot à lautre. * Expédition à température ambiante (les tests de stabilité montrent que ce produit peut être expédié sans aucune mesure de refroidissement.) |
|||||||||||
Préparation des solutions mères
Activité biologique
| Description | Le 3-Methyladenine (3-MA) est un inhibiteur sélectif de PI3K pour Vps34 et PI3Kγ avec une IC50 de 25 μM et 60 μM dans les cellules HeLa. Il bloque de manière consistente la PI3K de classe I, tandis que la suppression de la PI3K de classe III est transitoire, et inhibe également la formation d'autophagosome. Les solutions sont instables et doivent être préparées juste avant utilisation. | ||||||
|---|---|---|---|---|---|---|---|
| Cibles |
|
||||||
| In vitro | La légère préférence du 3-Methyladenine (3-MA) pour la prévention de Vps34 provient probablement d'un anneau hydrophobe spécifique à Vps34, qui encercle le groupe 3-méthyle de ce composé. Il a été rapporté qu'il provoque la mort des cellules cancéreuses dans des conditions normales et de famine, et qu'il pourrait également supprimer la migration et l'invasion cellulaires indépendamment de sa capacité à inhiber Autophagy, ce qui implique qu'il possède des fonctions autres que la suppression de l'Autophagy. Ce composé provoque une mort cellulaire dépendante des caspases, indépendamment de l'inhibition de l'Autophagy. Le traitement avec 5 mM de celui-ci réduit le pourcentage de cellules HeLa privées de glucose présentant des points GFP-LC3 à 23%. Les niveaux de LC3-I augmentent et les niveaux de LC3-II diminuent entre 12 et 48 heures dans les cellules traitées avec 3-MA. La conversion de LC3-I en LC3-II est supprimée par le composé. Le traitement des cellules HeLa avec 2,5 mM ou 5 mM pendant un jour n'affecte pas la viabilité cellulaire, tandis que le traitement avec 10 mM pendant un jour entraîne une diminution de 25,0% de la viabilité cellulaire. Le traitement des cellules avec 2,5, 5 ou 10 mM pendant deux jours entraîne une diminution de 11,5%, 38,0% et 79,4% de la viabilité, respectivement. Il diminue la viabilité cellulaire de manière dépendante du temps et de la dose, et raccourcit significativement la durée de l'arrêt prométaphase induit par le nocodazole. La suppression de l'Autophagy par 3-MA inhibe la mort cellulaire induite par SU11274. Un traitement prolongé avec celui-ci (jusqu'à 9 heures) induit une conversion significative de LC3 I en II dans les MEF de type sauvage. Un traitement prolongé avec 3-MA, mais pas la wortmannine, augmente nettement la ponctuation/agrégation de GFP-LC3. Sa conversion de LC3 induite et la libération de GFP libre sont dépendantes d'ATG7. Le traitement avec celui-ci entraîne une augmentation évidente du niveau de protéine p62. Le composé augmente le niveau de p62 même dans les MEF Atg5−/− ainsi que dans les cellules avec délétion d'ATG5 médiatisée par la DOX. Il inhibe la PI3K de classe I et de classe III selon des schémas temporels différents. Sa conversion induite de LC3 I en LC3 II est considérablement compromise dans les cellules Tsc2−/− par rapport aux cellules de type sauvage. Ce composé perturbe la fonction anti-autophagique du complexe mTOR 1. |
||||||
| In Vivo | Le 3-Methyladenine (3-MA) bloque l'Autophagy par son effet sur la phosphatidylinositol 3-kinase (PI3K) de classe III. Le traitement avec ce composé n'altère pas le degré d'hémorragie par rapport au groupe hémorragie sous-arachnoïdienne (SAH). Son prétraitement aggrave significativement les symptômes neurologiques par rapport au groupe SAH + véhicule. L'Autophagy est diminuée lors de son application. Inversement, la caspase-3 clivée est nettement régulée à la hausse dans le groupe SAH + 3-MA. Conformément à la régulation à la hausse de l'expression de la caspase-3 clivée, le nombre de cellules TUNEL-positives dans le cortex droit est significativement augmenté dans le groupe SAH + 3-MA par rapport au groupe SAH + véhicule. |
Protocole (de référence)
| Test kinase : |
|
|---|---|
| Test cellulaire : |
|
| Étude animale : |
|
Références
|
Validation du produit par le client
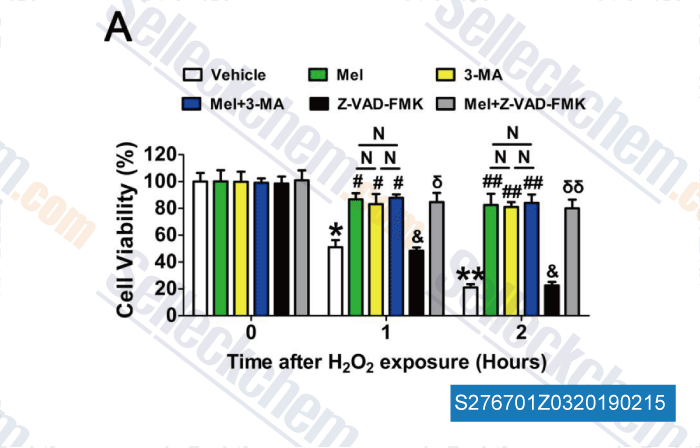
-
Données de [ , , Redox Biol, 2018, 18:138-157 ]
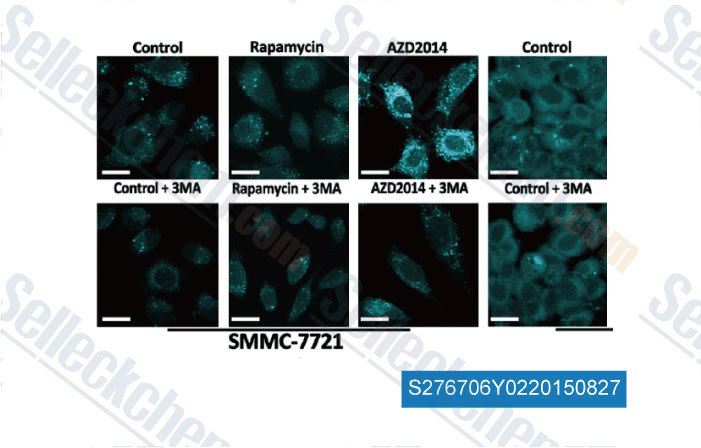
-
Données de [ , , Am J Cancer Res, 2015, 5(1): 125-139 ]
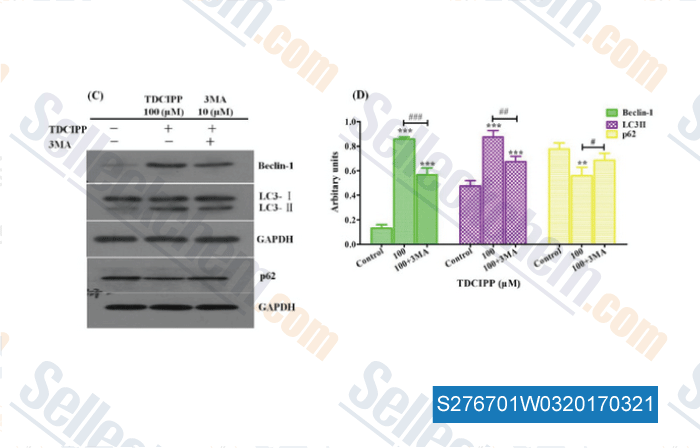
-
Données de [ , , Food Chem Toxicol, 2017, 100:183-196 ]
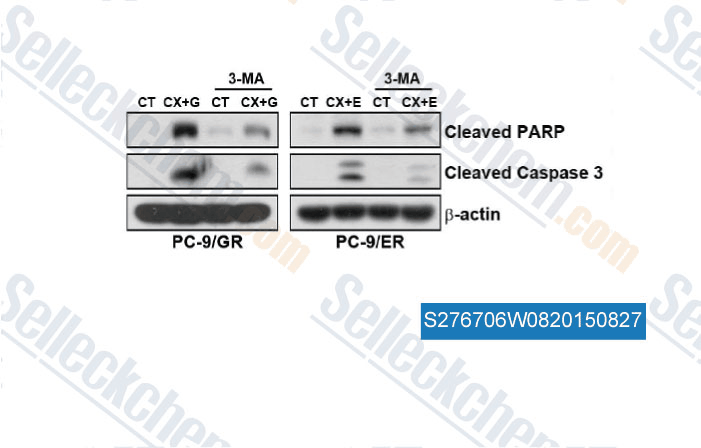
-
Données de [ , , PLoS One, 2014, 9(12): e114000 ]
De Selleck 3-Methyladenine (3-MA) A été cité par 978 Publications
| Cooperative nutrient scavenging is an evolutionary advantage in cancer [ Nature, 2025, 10.1038/s41586-025-08588-w] | PubMed: 39972131 |
| Host glutathione is required for Rickettsia parkeri cell division and intracellular survival [ Nat Commun, 2025, 16(1):5547] | PubMed: 40593553 |
| Viruses hijack FPN1 to disrupt iron withholding and suppress host defense [ Nat Commun, 2025, 16(1):5912] | PubMed: 40595467 |
| RNF167 mediates atypical ubiquitylation and degradation of RLRs via two distinct proteolytic pathways [ Nat Commun, 2025, 16(1):1920] | PubMed: 39994288 |
| Unfolded protein response kinase PERK supports survival and metastasis of circulating tumor cell clusters via SAM synthesis and H3K4me3-dependent PDGFB signaling [ Cancer Commun (Lond), 2025, 45(12):1706-1733.] | PubMed: 41212905 |
| Extracellular LCN2 Binding to 24p3R in Astrocytes Impedes α-Synuclein Endocytosis in Parkinson's Disease [ Adv Sci (Weinh), 2025, 12(39):e01694] | PubMed: 40686313 |
| USP10 Inhibits Ferroptosis via Deubiquinating POLR2A in Head and Neck Squamous Cell Carcinoma [ Adv Sci (Weinh), 2025, 12(36):e12271] | PubMed: 40605431 |
| Disrupting AGR2/IGF1 paracrine and reciprocal signaling for pancreatic cancer therapy [ Cell Rep Med, 2025, 6(2):101927] | PubMed: 39914384 |
| TBK1 is a signaling hub in coordinating stress-adaptive mechanisms in head and neck cancer progression [ Autophagy, 2025, 1-23.] | PubMed: 40114316 |
| H3K36me2 methyltransferase NSD2/WHSC1 promotes triple-negative breast cancer metastasis via activation of ULK1-dependent autophagy [ Autophagy, 2025, 21(8):1824-1842] | PubMed: 40097917 |
POLITIQUE DE RETOUR
La politique de retour inconditionnelle de Selleck Chemical garantit une expérience dachat en ligne fluide à nos clients. Si vous nêtes en aucun cas satisfait de votre achat, vous pouvez retourner tout article dans les 7 jours suivant sa réception. En cas de problèmes de qualité du produit, quil sagisse de problèmes liés au protocole ou au produit, vous pouvez retourner tout article dans les 365 jours suivant la date dachat initiale. Veuillez suivre les instructions ci-dessous lors du retour des produits.
EXPÉDITION ET STOCKAGE
Les produits Selleck sont transportés à température ambiante. Si vous recevez le produit à température ambiante, soyez assuré que le service dinspection de la qualité de Selleck a mené des expériences pour vérifier que le placement à température normale pendant un mois naffectera pas lactivité biologique des produits en poudre. Après réception, veuillez stocker le produit conformément aux exigences décrites dans la fiche technique. La plupart des produits Selleck sont stables dans les conditions recommandées.
NON DESTINÉ À UN USAGE HUMAIN, VÉTÉRINAIRE DIAGNOSTIQUE OU THÉRAPEUTIQUE.
