Technische gegevens
| Formule | C23H18ClF2N3O3S |
||||||
| Molecuulgewicht | 489.92 | CAS-nr. | 918504-65-1 | ||||
| Oplosbaarheid (25°C)* | In vitro | DMSO | 98 mg/mL (200.03 mM) | ||||
| Water | Insoluble | ||||||
| Ethanol | Insoluble | ||||||
| In Vivo (Voeg oplosmiddelen afzonderlijk en in volgorde toe aan het product.) |
|
||||||
|
* <1 mg/ml betekent licht oplosbaar of onoplosbaar. * Houd er rekening mee dat Selleck de oplosbaarheid van alle verbindingen intern test en de werkelijke oplosbaarheid enigszins kan afwijken van gepubliceerde waarden. Dit is normaal en is te wijten aan lichte batch-tot-batch variaties. * Verzending op kamertemperatuur (Stabiliteitstests tonen aan dat dit product zonder koelmaatregelen kan worden verzonden.) |
|||||||
Voorbereiden van stamoplossingen
Biologische activiteit
| Beschrijving | Vemurafenib (PLX4032, RG7204, RO5185426) is een nieuwe en potente remmer van B-RafV600E met een IC50 van 31 nM in een celvrije test. 10-voudig selectief voor B-RafV600E boven wild-type B-Raf in enzymatische tests en de cellulaire selectiviteit kan 100-voudig overschrijden. Vemurafenib (PLX4032, RG7204) induceert autophagy. | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Doelen |
|
|||||||||||
| In vitro | Vemurafenib (PLX4032) remt B-RAFV600E, C-RAF, evenals wildtype B-RAF, met IC50 van respectievelijk 31 nM, 48 nM en 100 nM. Deze verbinding remt ook verschillende niet-RAF kinases, waaronder ACK1, KHS1 en SRMS, met IC50 van 18 nM tot 51 nM. In melanoomcellijnen hangt het remmende effect ervan af van de B-RAF-mutatiestatus, omdat het diegenen die B-RAF V600-mutanten bevatten, waaronder V600E, V600D, V600K en V600R, potent remt, maar niet wildtype of andere mutanten. De IC50-waarden op deze cellen, waaronder MALME-3M, Colo829, Colo38, A375, SK-MEL28 en A2058, variëren van 20 nM tot 1 μM. In deze cellen remt Vemurafenib (0,1 μM tot 30 μM) ook de fosforylering van zowel MEK1/2 als ERK1/2. Het is zeer effectief bij de behandeling van melanoom, vanwege zijn vermogen om B-RAFV600E te remmen. Deze verbinding vertoont echter een beperkt effect bij patiënten met darmkanker die ook het B-RAFV600E oncoproteïne dragen. De reden hiervoor is dat in darmkankercellen de B-RAFV600E-remming door dit middel resulteert in een snelle feedback-EGFR-activering, die de PLX4032-geremde celproliferatie compenseert. | |||||||||||
| In Vivo | In B-RAFV600E-mutante muizen-xenograftmodellen remt Vemurafenib (PLX4032) (6 mg/kg–20 mg/kg) de tumorgroei. In muizen-xenograftmodellen van LOX-, Colo829- en A375-cellen remt deze verbinding (12,5 mg/kg–100 mg/kg) de tumorgroei en verlengt de overleving van de muizen. | |||||||||||
| Functies | Een nieuwe en potente remmer van het B-RAFV600E oncoproteïne. |
Protocol (uit referentie)
| Kinase-assay: |
|
|---|---|
| Celassay: |
|
| Dierstudie: |
|
Referenties
|
Klantproductvalidatie
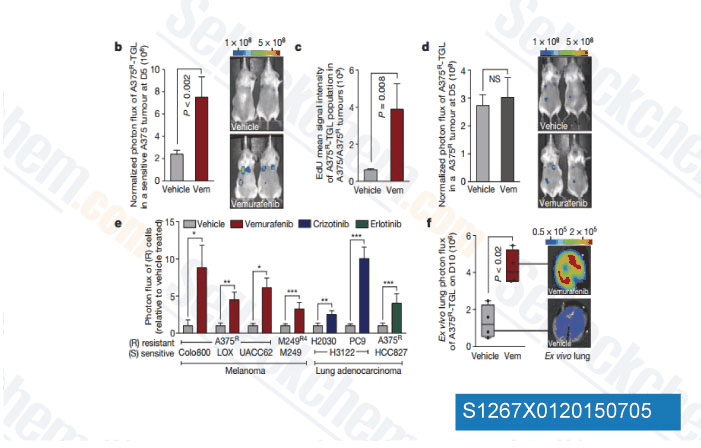
-
Gegevens van [ Nature , 2015 , 520(7547), 368-72 ]
![FRA1 downregulation during RAFi treatment drives the reactive secretome. c, Relative mRNA levels of FRA1 during vemurafenib exposure [0.1-1 uM]. d, Representative immunofluorescence staining of A375/A375R tumours for GFP (A375R, green) and FRA1 (red) after vehicle or vemurafenib treatment (5 days). DAPI, 49,6-diamidino-2-phenylindole. Scale bars, 50 um.](https://file.selleckchem.com/downloads/review/700px/Vemurafenib-S1267X0220150705.gif)
-
Gegevens van [ Nature , 2015 , 520(7547), 368-72 ]

-
Gegevens van [ Oncogene , 2015 , 10.1038/onc.2015.97 ]

-
Gegevens van [ Nature , 2014 , 508(7494), 118-22 ]
Sellecks PLX4032 (Vemurafenib) Is geciteerd door 714 Publicaties
| Pan-inhibition of super-enhancer-driven oncogenic transcription by next-generation synthetic ecteinascidins yields potent anti-cancer activity [ Nat Commun, 2025, 16(1):512] | PubMed: 39779693 |
| Blocking interplay between TERT and c-Myc: a new therapeutic strategy for BRAFV600E/pTERT double mutated tumors [ Int J Biol Sci, 2025, 21(11):4961-4978] | PubMed: 40860184 |
| Downregulated ALDH2 Contributes to Tumor Progression and Targeted Therapy Resistance in Human Metastatic Melanoma Cells [ Cells, 2025, 14(12)913] | PubMed: 40558540 |
| Inter-Relationship Between Melanoma Vemurafenib Tolerance Thresholds and Metabolic Pathway Choice [ Cells, 2025, 14(12)923] | PubMed: 40558548 |
| Exploiting Paradoxical Activation of Oncogenic MAPK Signaling by Targeting Mitochondria to Sensitize NRAS Mutant-Melanoma to Vemurafenib [ Int J Mol Sci, 2025, 26(6)2675] | PubMed: 40141318 |
| Acquired resistance to vemurafenib restrains thyroid cancer stem cell self-renewal by suppressing STAT3 activation [ Cell Signal, 2025, 133:111845] | PubMed: 40345509 |
| Dihydrotanshinone I enhanced BRAF mutant melanoma treatment efficacy by inhibiting the STAT3/SOX2 signaling pathway [ Front Oncol, 2025, 15:1429018] | PubMed: 39944829 |
| Suppression of Sebum Production by Vemurafenib Through Paradoxical ERK Activation Resulted in the Inhibition of the mTOR Pathway in 5α-Dihydrotestosterone-Differentiated Hamster Sebocytes In Vitro [ Exp Dermatol, 2025, 34(8):e70150] | PubMed: 40817681 |
| Selective inhibition of p300 by a novel small molecule EPS496 promotes cell death in vemurafenib-resistant BRAFV600E mutated melanoma cells [ Biochem Biophys Res Commun, 2025, 750:151382] | PubMed: 39884005 |
| Increased Mitochondrial Superoxide Level Is Partially Associated With Vemurafenib-Induced Renal Tubular Toxicity [ Basic Clin Pharmacol Toxicol, 2025, 136(4):e70015] | PubMed: 40018909 |
RETOURBELEID
Selleck Chemicals onvoorwaardelijke retourbeleid zorgt voor een soepele online winkelervaring voor onze klanten. Als u op enigerlei wijze ontevreden bent met uw aankoop, kunt u elk artikel(en) binnen 7 dagen na ontvangst retourneren. In geval van problemen met de productkwaliteit, zowel protocolgerelateerde als productgerelateerde problemen, kunt u elk artikel(en) binnen 365 dagen na de oorspronkelijke aankoopdatum retourneren. Volg de onderstaande instructies bij het retourneren van producten.
VERZENDING EN OPSLAG
Selleck producten worden bij kamertemperatuur vervoerd. Als u het product op kamertemperatuur ontvangt, wees dan gerust, de Selleck kwaliteitsinspectieafdeling heeft experimenten uitgevoerd om te controleren of de normale temperatuurplaatsing van één maand de biologische activiteit van poederproducten niet beïnvloedt. Na ontvangst dient u het product op te slaan volgens de vereisten beschreven in het gegevensblad. De meeste Selleck producten zijn stabiel onder de aanbevolen omstandigheden.
NIET VOOR HUMANE, VETERINAIRE DIAGNOSTISCHE OF THERAPEUTISCHE DOELEINDEN.
