Technische gegevens
| Formule | C19H20F3IN2O5S |
||||||
| Molecuulgewicht | 572.34 | CAS-nr. | 923032-37-5 | ||||
| Oplosbaarheid (25°C)* | In vitro | DMSO | 100 mg/mL (174.72 mM) | ||||
| Ethanol | 100 mg/mL (174.72 mM) | ||||||
| Water | Insoluble | ||||||
| In Vivo (Voeg oplosmiddelen afzonderlijk en in volgorde toe aan het product.) |
|
||||||
|
* <1 mg/ml betekent licht oplosbaar of onoplosbaar. * Houd er rekening mee dat Selleck de oplosbaarheid van alle verbindingen intern test en de werkelijke oplosbaarheid enigszins kan afwijken van gepubliceerde waarden. Dit is normaal en is te wijten aan lichte batch-tot-batch variaties. * Verzending op kamertemperatuur (Stabiliteitstests tonen aan dat dit product zonder koelmaatregelen kan worden verzonden.) |
|||||||
Voorbereiden van stamoplossingen
Biologische activiteit
| Beschrijving | Refametinib (RDEA119, Bay 86-9766) is een krachtige, ATP-onafhankelijke en zeer selectieve remmer van MEK1 en MEK2 met een IC50 van respectievelijk 19 nM en 47 nM. | ||||
|---|---|---|---|---|---|
| Doelen |
|
||||
| In vitro | Refametinib (RDEA119) bindt selectief en direct aan een allosterische pocket in de MEK1/2-enzymen, en is zeer werkzaam in het remmen van celproliferatie in verschillende tumorcellijnen, waaronder A375, SK-MEI-28, Colo205, HT-29 en BxPC3. Het remt de aanhechting-afhankelijke groei van menselijke kankercellijnen die de gain-of-function V600E BRAF-mutant bevatten, met GI50-waarden variërend van 67 tot 89 nM. Onder aanhechting-onafhankelijke omstandigheden zijn de GI50-waarden voor alle geteste cellijnen vergelijkbaar (40-84 nM). Deze verbinding vertoont een weefselselectiviteit die het potentieel voor bijwerkingen gerelateerd aan het centrale zenuwstelsel vermindert. Het remt potentieel de proliferatie van de 4 cellijnen die de BRAF-mutatie bevatten, maar heeft geen of bescheiden effecten op de andere 4 cellen die wild-type BRAF bevatten (IC50 van 0,034-0,217 μM versus 1,413-34,120 μM). Het remmende effect van Refametinib in geselecteerde cellijnen OCUT1 (BRAF V600E(+), PIK3CA H1047R(+)) en SW1376 (BRAF V600E(+)) wordt versterkt door combinatie met de mTOR-remmer, temsirolimus. Het en temsirolimus vertonen ook synergetische effecten op autofagische dood van selectief geteste OCUT1- en KAT18-cellen. | ||||
| In Vivo | Orale toediening van RDEA119 in een dosis van 50 mg/kg eenmaal daags gedurende 14 dagen leidt tot een 68% tumorgroeiremming (TGI) in het humane melanoom A375 tumormodel. Deze verbinding in een dosis van 25 mg/kg eenmaal daags gedurende 14 dagen resulteert in een 123% TGI in het humane coloncarcinoom Colo205 tumormodel (TGI > 100% treedt op wanneer de tumor krimpt tot onder het startvolume). Een dosis van 25 mg/kg eenmaal daags gedurende 14 dagen produceert respectievelijk 56% en 67% TGI voor HT-29- en A431-tumoren. |
Protocol (uit referentie)
| Kinase-assay: |
|
|---|---|
| Celassay: |
|
| Dierstudie: |
|
Referenties
|
Klantproductvalidatie

-
Gegevens van [ , , J Neurosci, 2012, 32(14): 4887-900 ]
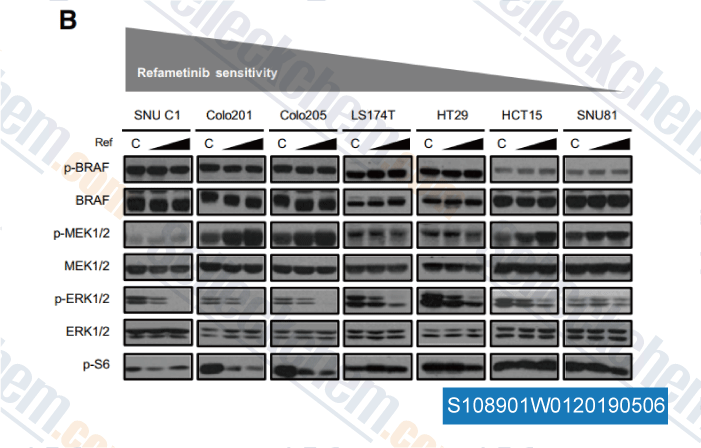
-
Gegevens van [ , , Mol Oncol, 2018, 12(8):1398-1409 ]
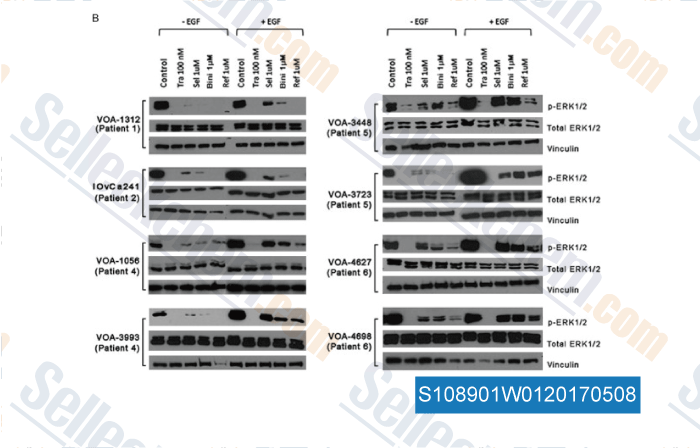
-
Gegevens van [ , , Am J Cancer Res, 2016, 6(10):2235-2251 ]
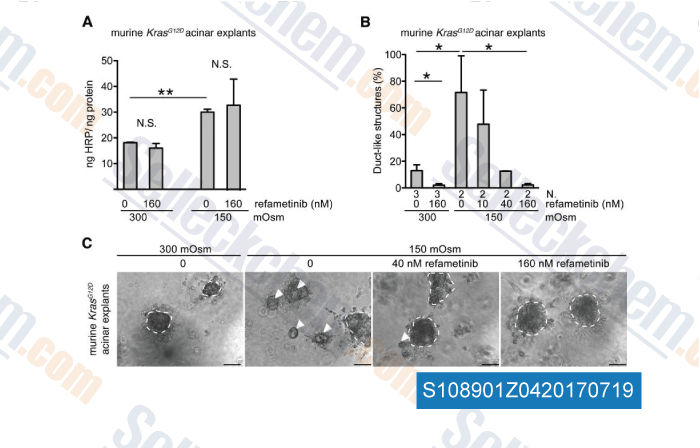
-
Gegevens van [ , , EBioMedicine, 2017, 15:90-99 ]
Sellecks Refametinib (RDEA119) Is geciteerd door 29 Publicaties
| System analysis links SMARCD3 regulons to growth signaling and MEK inhibitor response in everolimus-resistant ER+ breast cancer cells [ Cell Rep Med, 2025, 6(11):102425] | PubMed: 41260207 |
| Histone deacetylase inhibitors promote breast cancer metastasis by elevating NEDD9 expression [ Signal Transduct Target Ther, 2023, 8(1):11] | PubMed: 36604412 |
| Salmonella effector SopB reorganizes cytoskeletal vimentin to maintain replication vacuoles for efficient infection [ Nat Commun, 2023, 14(1):478] | PubMed: 36717589 |
| Signaling-induced systematic repression of miRNAs uncovers cancer vulnerabilities and targeted therapy sensitivity [ Cell Rep Med, 2023, S2666-3791(23)00367-1] | PubMed: 37734378 |
| Signaling-induced systematic repression of miRNAs uncovers cancer vulnerabilities and targeted therapy sensitivity [ Cell Rep Med, 2023, 4(10):101200] | PubMed: 37734378 |
| Protein Tyrosine Phosphatase Non-Receptor 11 (PTPN11/Shp2) as a Driver Oncogene and a Novel Therapeutic Target in Non-Small Cell Lung Cancer (NSCLC) [ Int J Mol Sci, 2023, 24(13)10545] | PubMed: 37445722 |
| Anatomic position determines oncogenic specificity in melanoma [ Nature, 2022, 604(7905):354-361] | PubMed: 35355015 |
| NOTCH signaling limits the response of Low Grade Serous Ovarian Cancers to MEK inhibition [ Mol Cancer Ther, 2022, MCT-22-0004] | PubMed: 36198031 |
| Secondary resistance to anti-EGFR therapy by transcriptional reprogramming in patient-derived colorectal cancer models [ Genome Med, 2021, 13(1):116] | PubMed: 34271981 |
| Targeting the PI3K and MAPK pathways to improve response to HER2-targeted therapies in HER2-positive gastric cancer [ J Transl Med, 2021, 19(1):184] | PubMed: 33933113 |
RETOURBELEID
Selleck Chemicals onvoorwaardelijke retourbeleid zorgt voor een soepele online winkelervaring voor onze klanten. Als u op enigerlei wijze ontevreden bent met uw aankoop, kunt u elk artikel(en) binnen 7 dagen na ontvangst retourneren. In geval van problemen met de productkwaliteit, zowel protocolgerelateerde als productgerelateerde problemen, kunt u elk artikel(en) binnen 365 dagen na de oorspronkelijke aankoopdatum retourneren. Volg de onderstaande instructies bij het retourneren van producten.
VERZENDING EN OPSLAG
Selleck producten worden bij kamertemperatuur vervoerd. Als u het product op kamertemperatuur ontvangt, wees dan gerust, de Selleck kwaliteitsinspectieafdeling heeft experimenten uitgevoerd om te controleren of de normale temperatuurplaatsing van één maand de biologische activiteit van poederproducten niet beïnvloedt. Na ontvangst dient u het product op te slaan volgens de vereisten beschreven in het gegevensblad. De meeste Selleck producten zijn stabiel onder de aanbevolen omstandigheden.
NIET VOOR HUMANE, VETERINAIRE DIAGNOSTISCHE OF THERAPEUTISCHE DOELEINDEN.
